题目内容
关于下列图象说法不正确的是( )
A、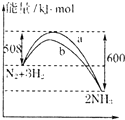 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 |
B、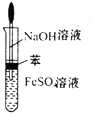 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 |
C、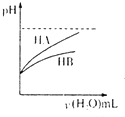 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB |
D、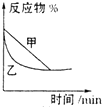 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
考点:反应热和焓变,化学平衡的影响因素,影响盐类水解程度的主要因素,制取氢氧化铁、氢氧化亚铁
专题:图示题
分析:A、由图可知,该反应放出的能量大于吸收的能量,所以为放热反应,热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ?mol-1;
B、Fe(OH)2很容易被空气中的氧气氧化,故制备Fe(OH)2时应用苯隔绝空气;
C、由图可知,稀释HA、HB两种酸的稀溶液时,HB的pH变化小,说明HB的酸性弱于HA的酸性,根据越弱越水解,同浓度的NaA溶液的pH小于NaB;
D、可逆反应2A(g)+2B(g)?3C(g)+D(s),反应气体体积减小,增大压强平衡向正反应方向移动,反应物%减小,平衡时,反应物%(甲)>反应物%(乙),与图象不相符.
B、Fe(OH)2很容易被空气中的氧气氧化,故制备Fe(OH)2时应用苯隔绝空气;
C、由图可知,稀释HA、HB两种酸的稀溶液时,HB的pH变化小,说明HB的酸性弱于HA的酸性,根据越弱越水解,同浓度的NaA溶液的pH小于NaB;
D、可逆反应2A(g)+2B(g)?3C(g)+D(s),反应气体体积减小,增大压强平衡向正反应方向移动,反应物%减小,平衡时,反应物%(甲)>反应物%(乙),与图象不相符.
解答:
解:A、由图可知,该反应放出的能量大于吸收的能量,所以为放热反应,热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-92kJ?mol-1,故A正确;
B、Fe(OH)2很容易被空气中的氧气氧化,故制备Fe(OH)2时应用苯隔绝空气,故B正确;
C、由图可知,稀释HA、HB两种酸的稀溶液时,HB的pH变化小,说明HB的酸性弱于HA的酸性,根据越弱越水解,同浓度的NaA溶液的pH小于NaB,故C正确;
D、可逆反应2A(g)+2B(g)?3C(g)+D(s),反应气体体积减小,增大压强平衡向正反应方向移动,反应物%减小,平衡时,反应物%(甲)>反应物%(乙),与图象不相符,故D错误;
故选D.
B、Fe(OH)2很容易被空气中的氧气氧化,故制备Fe(OH)2时应用苯隔绝空气,故B正确;
C、由图可知,稀释HA、HB两种酸的稀溶液时,HB的pH变化小,说明HB的酸性弱于HA的酸性,根据越弱越水解,同浓度的NaA溶液的pH小于NaB,故C正确;
D、可逆反应2A(g)+2B(g)?3C(g)+D(s),反应气体体积减小,增大压强平衡向正反应方向移动,反应物%减小,平衡时,反应物%(甲)>反应物%(乙),与图象不相符,故D错误;
故选D.
点评:本题考查了热化学方程式,催化剂对速率、平衡及能量的影响,压强对速率的影响,涉及的知识点较多,难度一般.

练习册系列答案
相关题目
下列溶液中能用来区别SO2和CO2气体的是( )
①澄清的石灰水 ②氢硫酸 ③氯水 ④酸性高锰酸钾溶液 ⑤氯化钡溶液 ⑥品红溶液.
①澄清的石灰水 ②氢硫酸 ③氯水 ④酸性高锰酸钾溶液 ⑤氯化钡溶液 ⑥品红溶液.
| A、①⑤ | B、③④⑤ |
| C、②⑥ | D、②③④⑥ |
下列说法不正确的是( )
| A、油脂属于酯类 |
| B、油脂的氢化又叫油脂的硬化 |
| C、淀粉和纤维素的通式都是(C6H10O5)n,是同分异构体 |
| D、葡萄糖能发生银镜反应 |
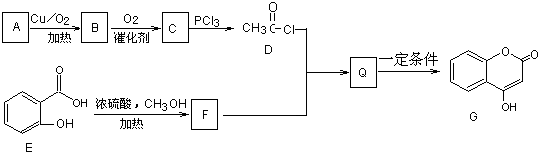
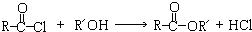
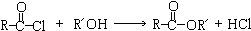 .
.
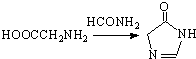
 .合成过程中无机试剂任选;合成路线流程图示例为:CH3CH2OH
.合成过程中无机试剂任选;合成路线流程图示例为:CH3CH2OH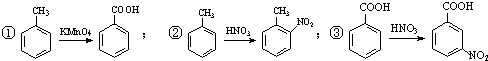
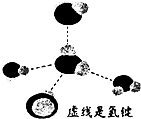 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
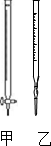 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤: