题目内容
在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中氧化剂与还原剂的物质的量之比是( )
| A、1:1 | B、3:8 |
| C、2:3 | D、8:3 |
考点:氧化还原反应的计算
专题:
分析:在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素的化合价升高,所以3molCu是还原剂,N元素的化合价降低,所以2mol硝酸是氧化剂,据此回答.
解答:
解:在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素的化合价升高,所以3molCu是还原剂,N元素的化合价降低,所以2mol硝酸是氧化剂,则氧化剂与还原剂的物质的量之比为2:3,
故选C.
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,氧化剂和还原剂的判断及计算的考查,注意从化合价角度分析,难度不大.

练习册系列答案
相关题目
下列离子方程式书写正确的是 ( )
| A、银氨溶液中加入足量盐酸产生沉淀[Ag(NH3)2]-+OH-+3H++Cl-═AgCl↓+2NH4++H2O |
| B、在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解3BaSO3+2H++2NO3-═3BaSO4↓+2NO↑+H2O |
| C、孔雀石可溶于盐酸 CO32-+2H+═CO2↑+H2O |
| D、氧化铁可溶于氢碘酸 Fe2O3+6H+═2Fe3++3H2O |
在某无色透明的且能使石蕊试剂变红的溶液中,能大量共存的离子组是( )
| A、K+、SO42-、HCO3- |
| B、K+、SO42-、NO3- |
| C、Fe2+、Cl-、NO3- |
| D、Fe3+、ClO-、Cl- |
下列装置图或曲线图与对应的叙述相符的是( )
A、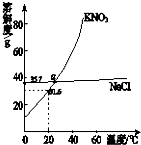 固体KNO3中混有NaCl,可用重结晶进行提纯 |
B、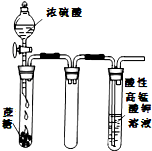 酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、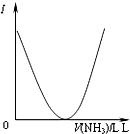 可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化 |
D、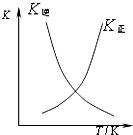 可表示在恒容密闭容器中反应“2SO2(g)+O2(g)═2SO3(g)△H<0”的平衡常数K正、K逆随温度 |
在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g.此混合气体中C和O两种原子的物质的量之比为( )
| A、4:3 | B、3:4 |
| C、2:1 | D、1:2 |
据报道,锌-空气电池将会成为21世纪理想动力源.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2+2H2O,下列有关锌-空气电池说法正确的是( )
| A、每生成1mol Na2ZnO2转移4mol电子 |
| B、负极反应式为:Zn+4OH--2e-=ZnO22-+2 H2O |
| C、电池工作时,溶液中的Na+向负级移动 |
| D、碱性或酸性电解液中,该电池正极反应式相同 |
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法错误的是( )
| A、若8>m>3,则X必定为主族元素 |
| B、若Y的气态氢化物化学式为YHn,且b=4,则该氢化物为非极性分子 |
| C、若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X |
| D、若a=b=3,8>m>n>b,则元素非金属性:X>Y |
化学与科技、社会生活有着密切的联系,下列有关说法正确的是( )
| A、2009年我国起征燃油税,工业上将石油分馏得到汽油,主要发生了化学变化 |
| B、2008年诺贝尔化学奖授予研究绿色荧光蛋白的科学家,区分蛋白质溶液和葡萄糖溶液可利用丁达尔效应 |
C、 “显世闻名”的奶粉事件中污染物为三聚氰胺(结构如图),其摩尔质量为l26g |
| D、2008年支援四川灾区的生活用品中食醋、纯碱、食盐的主要化学物质分别属于酸、碱、盐 |