题目内容
某元素的同位素![]() ,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应.若这种同位素原子核内有20个中子,求:
,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完全反应.若这种同位素原子核内有20个中子,求:
(1)Z值和A值.
(2)X元素在周期表中的位置.
(3)把X的单质放入水中,有何现象?写出反应的化学方程式.
答案:
解析:
解析:
|
答案:(1)Z=20 A=40 (2)第四周期,ⅡA族 (3)有气泡产生Ca+2H2O→Ca(OH)2+H2↑ 解析:设X的相对原子质量为A,则 XCl2+2AgNO3 A+71 2 1.11 g 1×0.02 求得A=40,其质子数为40-20=20,为Ca. |

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
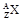 ,它的氯化物XCl21.11g溶于水制成溶液后, 加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl21.11g溶于水制成溶液后, 加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求: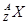 ,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的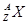 ,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求: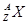 ,它的氯化物XCl2
2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2
2.22g溶于水制成溶液后,加入2mol/L的