题目内容
关于由锌片、铜片和稀硫酸组成的原电池的说法中,正确的是( )
| A、锌片作负极,发生还原反应 |
| B、电流方向是由锌片流向铜片 |
| C、锌片质量逐渐减少,铜片上有气泡产生 |
| D、电解质溶液的氢离子浓度保持不变 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在用锌片、铜片和稀硫酸组成的原电池装置中,锌片的活泼性大于铜片的活泼性,所以锌片作负极,负极上锌失电子发生氧化反应,铜片作正极,正极上氢离子得电子发生还原反应,以此解答该题.
解答:
解:A.锌易失电子发生氧化反应而作负极,故A错误;
B.电流从正极铜沿导线流向负极锌,故B错误;
C.锌、铜和稀硫酸构成的原电池中,锌易失电子生成锌离子进入溶液而质量逐渐减少,铜电极上氢离子得电子生成氢气而产生气泡,故C正确;
D.正极上氢离子得电子生成氢气,导致溶液中氢离子浓度减小,故D错误.
故选C.
B.电流从正极铜沿导线流向负极锌,故B错误;
C.锌、铜和稀硫酸构成的原电池中,锌易失电子生成锌离子进入溶液而质量逐渐减少,铜电极上氢离子得电子生成氢气而产生气泡,故C正确;
D.正极上氢离子得电子生成氢气,导致溶液中氢离子浓度减小,故D错误.
故选C.
点评:本题考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池的组成条件和工作原理,把握电极的判断和电极方程式的书写,难度不大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
为实现“绿色奥运”,下列环保建议中,你认为不能采纳的是( )
| A、开发、使用新能源 |
| B、用天然气代替汽油和柴油作发动机燃料 |
| C、禁止未经处理的工业废水和生活污水的任意排放 |
| D、大量使用农药,提高粮食产量 |
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
一定温度下,在一个固定容积的密闭容器中,可逆反应 A(S)+2B(g)?4C(g)△H>0达到平衡时,若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是( )
一定温度下,在一个固定容积的密闭容器中,可逆反应 A(S)+2B(g)?4C(g)△H>0达到平衡时,若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是( )
| A、增加A的物质的量 | B、加压 |
| C、升温 | D、使用催化剂 |
下列有机物的结构简式书写正确的是( )
A、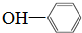 |
B、 |
| C、CH2=CH2-CH3 |
| D、CH3-C-O-O-C2H5 |
 某原电池装置如图所示,下列有关该电池中的铜电极的说法正确的是( )
某原电池装置如图所示,下列有关该电池中的铜电极的说法正确的是( )| A、该电极是正极 |
| B、电子从该电极流出 |
| C、该电极发生氧化反应 |
| D、该电极会逐渐溶解 |


