题目内容
7.固氮途径主要有生物固氮、大气固氮和工业固氮,下列不属于固氮反应的是( )| A. | 闪电时,氮气与氧气反应 | B. | 合成氨反应 | ||
| C. | 用氨气合成尿素 | D. | 金属镁在氮气中燃烧生成Mg3N2 |
分析 固氮是将大气中的游离态的氮转化为氮的化合物的过程,固氮也就是单质氮变成化合态的氮,由此分析解答.
解答 解:A、闪电时,氮气与氧气反应,生成一氧化氮,游离态的氮转化为化合态的氮,属固氮,故A不选;
B、合成氨反应是将氮气变成氨气,游离态的氮转化为化合态的氮,属固氮,故B不选;
C、用氨气合成尿素,化合态变成化合态,不属固氮,故C选;
D、金属镁在氮气中燃烧生成Mg3N2,游离态的氮转化为化合态的氮,属固氮,故D不选;
故选C.
点评 本题考查氮的固定,实质上就是分析元素化合价的变化,学生要熟记氮的转化原理是解题的关键,比较容易.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 生物质能来源于植物机体加工产品所贮存的能量,绿色植物通过光合作用将化学能转化为生物质能 | |
| B. | 铝硅酸盐分子筛可用于物质分离,还可用作干燥剂、催化剂及催化剂载体 | |
| C. | 人体从食物中摄取蛋白质,在体内先水解成各种氨基酸,经过不断的分解,最终生成水和二氧化碳排出体外 | |
| D. | 铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的杀菌消毒 |
15. NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
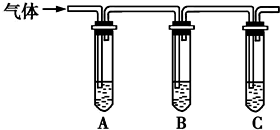
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过如图所示装置检验气体的成分,从而判断该消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI-淀粉溶液、1.0mol•L-1NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案(如图).
(3)用滴定法测定消毒液中NaClO的浓度.实验步骤如下:
①量取 25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②滴定分析.将c mol•L-1的酸性KMnO4溶液装入酸式(填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据.重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{2ab-5vc}{50}$mol•L-1(用含a、b、c、V的代数式表示).
 NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过如图所示装置检验气体的成分,从而判断该消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI-淀粉溶液、1.0mol•L-1NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案(如图).
| 所加试剂 | 预期现象和结论 |
| 向试管A中加足量①1.0mol/LK淀粉溶液; 试管B中加1%品红溶液; 试管C中加②澄清石灰水. | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质; ③若A中溶液变蓝色,B中溶液不退色(无变化),C中溶液不变浑浊(无变化),则消毒液未变质,则消毒液未变质; ④若A中溶液不变蓝色(无变化),B中溶液不退色(无变化),C中溶液变浑浊则消毒液完全变质,则消毒液完全变质. |
①量取 25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②滴定分析.将c mol•L-1的酸性KMnO4溶液装入酸式(填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据.重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{2ab-5vc}{50}$mol•L-1(用含a、b、c、V的代数式表示).
2.下列有关物质用途的叙述中,不正确的是( )
| A. | 硅可用作制造变压器的铁芯材料 | |
| B. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| C. | 二氧化硅可用于制造光导纤维 | |
| D. | 石英玻璃可用于制造光学仪器 |
19.下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
| A. | 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c( HC2O4-)+c( C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
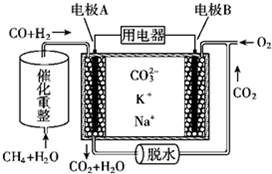
16.一种熔融碳酸盐燃料电池原理示意如图所示
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 电池工作时,K+向B极移动 | |
| B. | 电极B上发生的电极反应:O2+2CO2+4e-═2CO32- | |
| C. | 电池工作时,CO2可以循环利用 | |
| D. | 消耗1molCH4催化重整得到的CO和H2通入电极A,需要电极B同时通入33.6L的O2 |
5.在日常生活中,下列解决问题的方法不可行的是( )
| A. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 为避免船体遭受腐蚀,在船身上装铅块 | |
| C. | 为增强治疗缺铁性贫血效果,可在口服硫酸亚铁片时同服维生素C | |
| D. | 为使水果保鲜,可在水果箱内放入高锰酸钾溶液浸泡过的硅藻土 |