题目内容
18.A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| B | C |
| D |
| A. | 简单离子的半径大小关系:C>E | |
| B. | D元素的气态氢化物比C元素的气态氢化物稳定 | |
| C. | 由A、B、C三种元素组成的离子化合物中,阴、阳离子个数比为1:1 | |
| D. | 由C、D、E三种元素组成的化合物只有一种 |
分析 A、B、C、D、E均为短周期主族元素,A是短周期中原子半径最小的元素,A为H元素;E是短周期中最活泼的金属元素,E为Na元素;A、B、C三种元素的原子序数之和等于D元素的原子序数,结合B、C、D在周期表中的位置,设C的原子序数为x,则1+x-1+x=x+8,则x=8,即B为N,C为O,D为S,以此来解答.
解答 解:由上述分析可知,A为H,B为N,C为O,D为S,E为Na,
A.具有相同电子排布的离子中,原子序数大的离子半径小,则简单离子的半径大小关系:C>E,故A正确;
B.非金属性O>S,则D元素的气态氢化物不如C元素的气态氢化物稳定,故B错误;
C.由A、B、C三种元素组成的离子化合物为硝酸铵,阴、阳离子个数比为1:1,故C正确;
D.由C、D、E三种元素组成的化合物有硫酸钠、亚硫酸钠等,故D错误;
故选BD.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、原子序数推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 我国古代四大发明之一黑火药由硫酸、硝酸和木炭按一定比例混合制成 | |
| B. | PH计不能用于酸碱中和滴定终点的判断 | |
| C. | 石油的分馏,煤的干馏、气化、液化均是物理变化 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
9.甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景.
(1)已知反应CO(g)+2H2(g)═CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如表:
则x=1076.
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:
CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1<0,
CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3.
(1)已知反应CO(g)+2H2(g)═CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如表:
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:
CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1<0,
CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3.
6.下表为元素周期表的一部分,请按要求回答问题:
(1)表中元素F的非金属性最强,元素Na的金属性最强(填元素符号).
(2)表中元素③的原子结构示意图 ;元素⑨形成的氢化物的电子式
;元素⑨形成的氢化物的电子式 .
.
(3)表中元素④、⑨形成的氢化物的稳定性顺序为HF>HCl(填化学式).
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为HClO4>H2SO4(填化学式).
(5)表中元素③、④、⑥、⑦的原子半径大小为Na>Mg>O>F(填元素符号).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中元素③的原子结构示意图
 ;元素⑨形成的氢化物的电子式
;元素⑨形成的氢化物的电子式 .
.(3)表中元素④、⑨形成的氢化物的稳定性顺序为HF>HCl(填化学式).
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为HClO4>H2SO4(填化学式).
(5)表中元素③、④、⑥、⑦的原子半径大小为Na>Mg>O>F(填元素符号).
13.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如下流程:

下列说法正确的是( )

下列说法正确的是( )
| A. | 溶解烧渣选用足量酸,可以从常见的强酸中选择任意一种,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,只需要缓慢加热至溶液出现少量晶体,停止加热利用余热蒸干即可 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
10.下列叙述正确的是( )
| A. | 非金属原子间以共价键结合的物质一定是共价化合物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 凡是能电离出离子的化合物一定是离子化合物 | |
| D. | 凡是含有离子键的化合物一定是离子化合物 |
7.根据表提供的数据可知,在溶液中能大量共存的微粒组是( )
| 化学式 | 电离常数 |
| CH3COOH | K=1.7×10-5 |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | H2CO3、HCO3-、CH3COO-、CN- | B. | HCO3-、CH3COOH、CN-、CO32- | ||
| C. | HCN、HCO3-、CN-、CO32- | D. | HCN、HCO3-、CH3COO-、CN- |
8.关于Na2CO3溶液,下列关系不正确的是( )
| A. | c(Na+)>2c(CO32-) | B. | c(Na+)=2 | ||
| C. | c(Na+)>c(CO32-)>c(OH-)>c(H+) | D. | c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
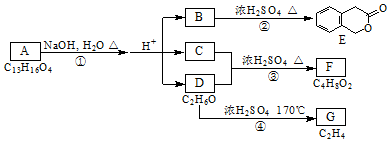
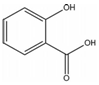 ,其名称为:邻羟基苯甲酸
,其名称为:邻羟基苯甲酸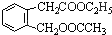 ④反应的反应类型是消去反应
④反应的反应类型是消去反应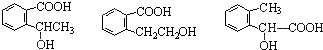 任意一个
任意一个 或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.
或CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH.