题目内容
下列表达式书写正确的是
A.CaCO3的电离方程式:CaCO3=Ca2++CO32-
B.HCO3-的电离方程式:HCO3-+H2O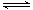 H3O++CO32-
H3O++CO32-
C.CO32-的水解方程式:CO32-+2H2O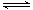 H2CO3+2OH-
H2CO3+2OH-
D.CaCO3的沉淀溶解平衡表达式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
【答案】
AB
【解析】
试题分析:A、碳酸钙难溶于水,但属于强电解质,因此CaCO3的电离方程式CaCO3=Ca2++CO32-,A正确;B、HCO3-是弱酸的酸式根,其电离方程式为HCO3-+H2O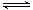 H3O++CO32-,B正确;C、CO32-是弱酸的酸根,因此CO32-的水解方程式为CO32-+H2O
H3O++CO32-,B正确;C、CO32-是弱酸的酸根,因此CO32-的水解方程式为CO32-+H2O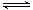 HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O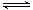 OH-+H2CO3,C不正确;D、溶解平衡是动态平衡,因此CaCO3的沉淀溶解平衡表达式为CaCO3(s)
OH-+H2CO3,C不正确;D、溶解平衡是动态平衡,因此CaCO3的沉淀溶解平衡表达式为CaCO3(s)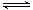 Ca2+(aq)+CO32-(aq),D不正确,答案选AB。
Ca2+(aq)+CO32-(aq),D不正确,答案选AB。
考点:考查电离方程式、水解方程式、溶解平衡表达式的正误判断

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
中学化学涉及多种常数,下列说法正确的是( )
| A、两种物质反应,不管怎样书写化学方程式,平衡常数不变 | ||
B、某温度下,2L密闭容器中加入4mol A和2mol B发生反应:3A(g)+2B(g)?4C(s)+2D( g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=
| ||
| C、温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | ||
| D、难溶电解质AB2饱和溶液中,c(A2+)=x mol?L-1,c(B-)=y mol?L-1,则Ksp值为4xy2 |
 4C(1)+2D( g)。平衡时测得n(C)=1.6mol ,反应的化学平衡常数表达式为
4C(1)+2D( g)。平衡时测得n(C)=1.6mol ,反应的化学平衡常数表达式为