题目内容
2.等物质的量的含氮化合物发生下列反应,转移电子数最少的是( )| A. | NO2和H2O | B. | NH3和O2 | C. | Fe和稀HNO3 | D. | NO和O2 |
分析 设含氮物质均为1mol,结合反应及元素的化合价变化计算转移电子,以此来解答.
解答 解:设含氮物质均为1mol,
A.二氧化氮与水反应生成硝酸和NO,转移电子为1mol×$\frac{1}{3}$×(4-2)=$\frac{2}{3}$mol;
B.氨气与氧气反应生成NO和水,转移电子为1mol×[2-(-3)]=5mol;
C.反应生成硝酸铁(或硝酸亚铁)、NO和水,生成硝酸铁时转移电子为1mol×$\frac{1}{4}$×(5-2)=$\frac{3}{4}$mol,生成硝酸亚铁时转移电子为1mol×$\frac{2}{8}$×(5-2)=$\frac{3}{4}$mol;
D.反应生成二氧化氮,转移电子为1mol×(4-2)=2mol,
显然A中转移电子最少,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
12. 2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )
2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )
 2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )
2015年2月科学家成功观察到CO与O形成化学键生成C02的全过程(CO和O附着在一种钌催化剂表面,用激光脉冲将其加热到2000K).下列说法不正确的是( )| A. | 该过程可以表示为:CO+O$\frac{\underline{\;催化剂\;}}{\;}$C02 | |
| B. | 该过程中有热量放出 | |
| C. | 催化剂能降低反应的活化能 | |
| D. | 钌催化剂能改变该反应的焓变 |
13.反应CO(g)+H2(g)?C(s)+H2O(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )①?将容器的体积缩小一半②?保持体积不变,充入He?③保持压强不变,充入He.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ② |
17.欲使Ca(OH)2悬浊液变澄清,可以选择加入的试剂是( )
| A. | CaCl2浓溶液 | B. | NaOH浓溶液 | C. | NH4Cl浓溶液 | D. | MgCl2浓溶液 |
7.已知25℃时有关弱酸的电离平衡常数:则下列反应的离子方程式正确的是( )
| HF | HClO | H2S | C6H5OH |
| Ki=3.53×l0-4 | Ki=2.95×l0-8 | K1=9.1×l0-8 K2=1.1×l0-12 | Ki=1.28×l0-10 |
| A. | ClO-+H2S→HClO+HS- | B. | H2S+2C6H5O-→2C6H5OH+S2- | ||
| C. | HF+C6H5O-→C6H5OH+F- | D. | HF(少量)+S2-→F-+HS- |
11.化学中部分物质既能和盐酸反应又能和氢氧化钠溶液反应,下列物质不具有这种性质的是( )
| A. | Al | B. | Al(OH)3 | C. | FeSO4 | D. | NaHCO3 |
12.对氕(H)、氘(D)、氚(T)相关知识叙述正确的是( )
| A. | 1molH、1molD、1molT各含中子数形同 | |
| B. | H2O、D2O、T2O的相对分子质量分别是18、20、22 | |
| C. | H、D、T属同种原子 | |
| D. | 在酸性条件下CH3COOHC2H5在D2O中水解,则反应混合物中所有内部肯定含有D原子 |
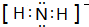 .
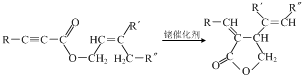
.
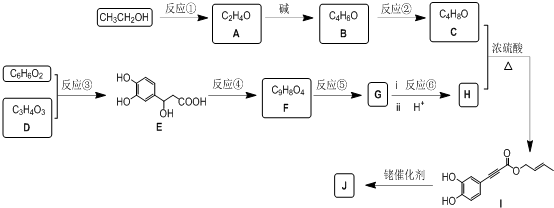
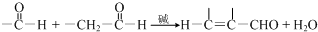
 任意一种.
任意一种.