题目内容
下列说法不正确的是( )
| A、室温下将CaO、Na2O、Na、NaOH各5克分别投入100克水中,充分搅拌后,所得溶液中溶质的质量分数最小的是CaO |
| B、正戊烷、异戊烷、新戊烷的熔沸点由高到低的顺序为新>异>正 |
| C、AlO2-、HCO3-、Na+、K+等离子不能在水溶液里大量共存 |
| D、将NaHCO3溶液和Na2SO3溶液分别蒸干灼烧,得到的固体都不是原溶质 |
考点:溶液中溶质的质量分数及相关计算,分子间作用力对物质的状态等方面的影响,离子共存问题,含硫物质的性质及综合应用
专题:计算题,基本概念与基本理论,元素及其化合物
分析:A.CaO与水反应生成氢氧化钙,氢氧化钙溶解度较小;
B.碳原子数相同,支链越多熔沸点越低;
C.AlO2-与HCO3-能发生双水解生成氢氧化铝和碳酸根离子,
D.NaHCO3不稳定,受热易分解,故蒸干灼烧,得到的固体是碳酸钠;Na2SO3易被氧化,故蒸干灼烧,得到的固体是硫酸钠.
B.碳原子数相同,支链越多熔沸点越低;
C.AlO2-与HCO3-能发生双水解生成氢氧化铝和碳酸根离子,
D.NaHCO3不稳定,受热易分解,故蒸干灼烧,得到的固体是碳酸钠;Na2SO3易被氧化,故蒸干灼烧,得到的固体是硫酸钠.
解答:
解:A.CaO与水反应生成氢氧化钙,氢氧化钙溶解度较小,故所得溶液中溶质的质量分数最小的是CaO,故A正确;
B.碳原子数相同,支链越多熔沸点越低,故正戊烷、异戊烷、新戊烷的熔沸点由高到低的顺序为正>异>新,故B错误;
C.AlO2-与HCO3-能发生双水解生成氢氧化铝和碳酸根离子,故不能共存,故C正确;
D.NaHCO3不稳定,受热易分解,故蒸干灼烧,得到的固体是碳酸钠;Na2SO3易被氧化,故蒸干灼烧,得到的固体是硫酸钠,故D正确;
故选B.
B.碳原子数相同,支链越多熔沸点越低,故正戊烷、异戊烷、新戊烷的熔沸点由高到低的顺序为正>异>新,故B错误;
C.AlO2-与HCO3-能发生双水解生成氢氧化铝和碳酸根离子,故不能共存,故C正确;
D.NaHCO3不稳定,受热易分解,故蒸干灼烧,得到的固体是碳酸钠;Na2SO3易被氧化,故蒸干灼烧,得到的固体是硫酸钠,故D正确;
故选B.
点评:本题考查质量分数、烃类熔沸点的比较、盐龙的水解、物质的稳定性等知识,知识点较多,难度中等.要注意基础知识的积累.

练习册系列答案
相关题目
实现以下变化,只需经过一步反应即可实现的是( )
| A、CuO→Cu(OH)2 |
| B、Al2O3→Al(OH)3 |
| C、SiO2→H2SiO3 |
| D、Fe→FeCl3 |
一定温度下,在2L的密闭容器中加入4molA和6molB,发生如下反应:2A(g)+3B(g)?4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L.下列说法正确的是( )
| A、前10min反应的平均速率V(C)=0.10mol/L?min |
| B、10min后向容器中加入A,重新平衡时A的转化率一定大于50% |
| C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L |
| D、反应达平衡时B的平衡浓度是1.5mol/L |
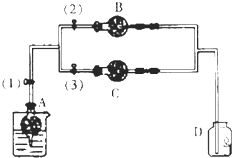 在干燥管A中的块状白色固体为某种正盐,B中为淡黄色粉末,C中为白色粉末,并将A、B、C按图所示连接.打开活塞(1)(3)时,D中蜡烛火焰熄灭,C中白色粉末变蓝;当打开活塞(1)(2)时,D中蜡烛火焰变得更明亮;关闭活塞(1)时,A中反应可自行停止.
在干燥管A中的块状白色固体为某种正盐,B中为淡黄色粉末,C中为白色粉末,并将A、B、C按图所示连接.打开活塞(1)(3)时,D中蜡烛火焰熄灭,C中白色粉末变蓝;当打开活塞(1)(2)时,D中蜡烛火焰变得更明亮;关闭活塞(1)时,A中反应可自行停止.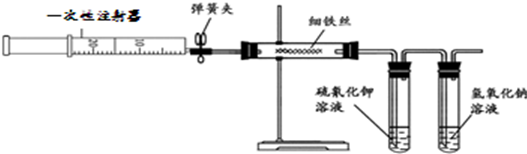
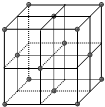 碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,
碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,