题目内容
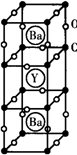 1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图.
1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图. (1)根据图1所示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比,确定其化学式为
(2)根据(1)所推出的化合物的组成,计算其中Cu原子的平均化合价(该化合物中各元素的化合价为Y3+,Ba2+,Cu2+和Cu3+)试计算化合物中这两种价态Cu原子个数比为
考点:晶胞的计算
专题:化学键与晶体结构
分析:(1)利用均摊法计算晶胞的结构;
(2)利用化合价代数和为0计算.
(2)利用化合价代数和为0计算.
解答:
解:(1)结合晶胞图再根据均摊法可知,在一个晶胞中含有Y原子数为1,Cu原子数为8×
+8×
=3,Ba原子数为2,O原子数为的个数为8×
+12×
=7,所以Y、Cu、Ba和O的个数比为1:3:2:7,所以化学式为YBa2Cu3O7;
故答案为:YBa2Cu3O7;
(2)根据化合价代数和为0可知,Cu的平均化合价为+
=+
,
设晶胞平均含有x个Cu2+,ygCu3+,
则有:
解之得x=2,y=1,
所以:Cu2+:Cu3+=2:1.
故答案为:Cu2+:Cu3+=2:1.
| 1 |
| 4 |
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
故答案为:YBa2Cu3O7;
(2)根据化合价代数和为0可知,Cu的平均化合价为+
| 2×7-3-2×2 |
| 3 |
| 7 |
| 3 |
设晶胞平均含有x个Cu2+,ygCu3+,
则有:
|
解之得x=2,y=1,
所以:Cu2+:Cu3+=2:1.
故答案为:Cu2+:Cu3+=2:1.
点评:本题考查晶胞的计算,题目难度中等,本题中注意电子排布式的书写以及晶胞的计算方法,为中学阶段常考查内容.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
某无色溶液加入氯化钡溶液后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中( )
| A、一定含有SO42- |
| B、一定含有Ag+ |
| C、可能含有SO42-或 SO32- 或Ag+ |
| D、一定含有Ag+、SO42 |
在甲、乙两烧杯溶液中,共含有Cu2+、K+、H+、Cl-、CO32-、OH-6种离子.已知甲烧杯的溶液含其中3种离子并呈蓝色,则乙烧杯的溶液中含有的另3种离子是( )
| A、Cu2+、H+、Cl- |
| B、K+、CO32-、Cl- |
| C、K+、OH-、CO32- |
| D、K+、H+、Cl- |
相同条件下,向等体积、pH=2的两种一元酸HA和HB的溶液中加入足量的镁粉,充分应后,收集到H2的体积前者大于后者,下列说法正确的是( )
| A、HA一定是强酸 |
| B、HB一定是强酸 |
| C、HB一定是弱酸 |
| D、反应开始时二者生成H2的速率相同 |
下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发.
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发.
| A、试管 | B、胶头滴管 |
| C、玻璃棒 | D、漏斗 |
下列仪器可以加热的是( )
①蒸馏烧瓶;②容量瓶;③蒸发皿;④试管;⑤表面皿;⑥分液漏斗;⑦量筒;⑧锥形瓶.
①蒸馏烧瓶;②容量瓶;③蒸发皿;④试管;⑤表面皿;⑥分液漏斗;⑦量筒;⑧锥形瓶.
| A、①③④⑧ | B、②④⑥⑧ |
| C、③④⑤ | D、②③④⑦ |
某溶液能溶解Al(OH)3,不能溶解SiO2,在该溶液中可以大量共存的离子组是( )
| A、I-、Na+、Cl-、NO3- |
| B、Fe3+、Ca2+、CH3COO-、HCO3- |
| C、Na+、Mg2+、NO3-、SO42- |
| D、Ba2+、K+、Cl-、SO42- |
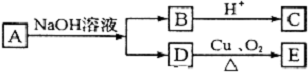 某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )
某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )