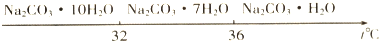题目内容
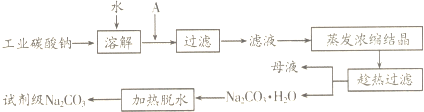
7.纯碱即soda,是一种重要的化工原料,是食品、造纸、制药、玻璃、肥皂、印染等工业乃至人民日常生活的必需品,工业制取方法有很多种.Ⅰ.布兰制碱法
古代,人们从草木灰中提取碳酸钾,后来又从盐碱地和盐湖等天然资源中获取碳酸钠,但量太小,远不能满足化工生产需求.1791年法国医生路布兰首先获得制碱专利,以食盐为原料制碱,称路布兰制碱法.
路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱.
(1)食盐和浓硫酸反应的化学方程式为2NaCl+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑;硫酸钠和焦炭、石灰石反应的化学方程式为Na2SO4+4C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+4CO或Na2SO4+2C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+2CO2(已知产物之一为CaS).
(2)该方法的缺点是该方法生产时需要高温,浓硫酸对设备腐蚀严重.
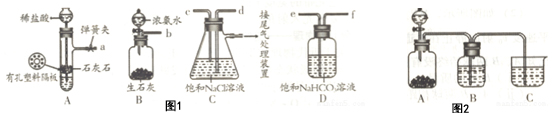
Ⅱ.氨碱法即索尔维制碱法,是1862年比利时人索尔维以食盐、氨、二氧化碳原料发明的制碱法,碱法的工艺如图1所示,得到的碳酸氢钠精短少生成纯碱.
(3)图中的中间产物BCO2,CCa(OH)2,DNH3(写化学式).
(4)装置乙中发生反应的化学方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl.
Ⅲ.候氏制碱法
我国化学家侯德榜对上述方法做了较大的改进,此法的最大特点是不从固体碳酸氢铵而是由盐卤先吸收氨后再碳酸化以进行连续生产,这样巧妙的把氨气工业和制碱工业联合起来,故又称联合制碱法.
(5)候氏制碱法的优点是提高食盐利用率、副产物氯化铵可用作化肥、可利用合成氨的产物CO2.
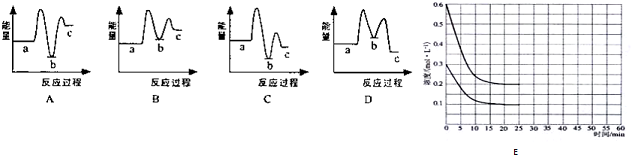
(6)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾.请结合图2的溶解度(S)随温度变化曲线,分析说明是否可行?不可行,碳酸氢钾的溶解度较大,降温过程中不会析出碳酸氢钾晶体.

分析 (1)浓硫酸为高沸点酸,能制取低沸点的酸氯化氢,食盐和浓硫酸反应生成氯化氢和硫酸钠;由题目信息可知,硫酸钠与石灰石、焦炭反应生成CaS、Na2CO3,根据元素守恒可知,还原C的氧化物CO或CO2生成;
(2)根据该方法选用试剂和条件判断;
(3)碳酸钙在石灰窑中加热分解生成CaO与CO2,故A为CaO,B为CO2,CaO在熟化桶内与水反应生成氢氧化钙;氢氧化钙与氯化铵在混合池内反应生成氨气与氯化钙;
(4)氨气与氯化钠溶液混合后,在乙中与二氧化碳发生反应,生成NaHCO3、NH4Cl;
(5)能提高原料的利用率,减少废渣的排放,保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高; NH4Cl 可做氮肥;可与合成氨厂联合,可利用合成氨的产物CO2;
(6)不可行.因为KHCO3和NH4Cl的溶解度相差不大,当温度高于40℃时,KHCO3的溶解度大于NH4Cl,降温结晶时会析出较多的KCl.
解答 解:(1)利用高沸点酸制备挥发性酸,且HCl极易溶于水,故利用直接使用浓硫酸和氯化钠制取氯化氢,反应为:2NaCl+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑,
由题目信息可知,硫酸钠与石灰石、焦炭反应生成CaS、Na2CO3,根据元素守恒可知,还原C的氧化物CO或CO2生成,故反应方程式为:Na2SO4+4C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+4CO或Na2SO4+2C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+2CO2,
故答案为:2NaCl+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑;Na2SO4+4C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+4CO或Na2SO4+2C+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaS+Na2CO3+2CO2;
(2)该方法选用浓硫酸在高温下反应,所以缺点为生产时需要高温,浓硫酸对设备腐蚀严重,故答案为:该方法生产时需要高温,浓硫酸对设备腐蚀严重;
(3)碳酸钙在石灰窑中加热分解生成CaO与CO2,故A为CaO,B为CO2,CaO在熟化桶内与水反应生成氢氧化钙,故C为Ca(OH)2;氢氧化钙与氯化铵在混合池内反应生成氨气与氯化钙,故D为NH3,
故答案为:CO2;Ca(OH)2;NH3;
(4)氨气与氯化钠溶液混合后,在乙中与二氧化碳发生反应,生成NaHCO3、NH4Cl,反应方程式为NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl,
故答案为:NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl;
(5)该方法能提高原料的利用率,减少废渣的排放,保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高;NH4Cl 可做氮肥;可与合成氨厂联合,可利用合成氨的产物CO2,
故答案为:提高食盐利用率、副产物氯化铵可用作化肥、可利用合成氨的产物CO2;
(6)由溶解曲线图可知KHCO3和NH4Cl的溶解度相差不大,当温度高于40℃时,由图象可知,降温结晶时会析出较多的KCl,无法大量析出碳酸氢钾;
故答案为:不可行; 碳酸氢钾的溶解度较大,降温过程中不会析出碳酸氢钾晶体.
点评 本题考查制碱法的工艺的流程,需要学生细读生产工艺图中各物质的变化进行解答,注意根据物质的主要性质分析工业装置和反应原理,题目难度中等.

| A. | 反应条件是加热的反应都是吸热反应 | |
| B. | 化学反应除了生成新的物质外,通常放出大量热 | |
| C. | 物质燃烧一定是放热反应 | |
| D. | 放热的化学反应不需要加热就能发生 |
| A. | 为避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为牺牲阳极的阴极保护法 | |
| B. | 原电池工作时,电流的方向由正极→负载→负极→原电池中电解质溶液→正极 | |
| C. | 纯银在空气中久置变黑发生的是化学腐蚀 | |
| D. | 在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液 |
| A. | 氢氧化钠溶液和稀盐酸反应:H++OH-═H2O | |
| B. | 大理石与盐酸反应制取二氧化碳:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁粉投入盐酸溶液中:2Fe+6H+═Fe3++3H2↑ | |
| D. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O |
| 阳离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
| A. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,滴加氢氧化钠溶液时Fe2+先产生沉淀 | |
| B. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,若除去混合溶液中的Fe2+、Fe3+,可先加入稀硝酸,再加入氧化铜调节溶液的pH的范围为3.2-4.7 | |
| C. | 相同温度下,Ksp[(Cu(OH)2)>Ksp[(Fe(OH)2) | |
| D. | 在含有Fe2+、Fe3+、Cu2+的混合溶液中,除去混合溶液中的Fe2+、Fe3+,可加入足量的铁粉 |