题目内容
室温下,若某溶液中由水电离产生的c(OH-)=1×10-15mol/L,则满足此条件的溶液中一定不可以大量共存的离子组是( )
| A、Fe2+、Na+、NO3-、Cl- |
| B、Al3+、Na+、Cl-、NO3- |
| C、K+、Na+、Cl-、AlO2- |
| D、K+、NH4+、SO42-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:由水电离产生的c(OH-)=1×10-15mol/L,该溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.酸性溶液中,亚铁离子和硝酸根离子发生氧化还原反应;碱性溶液中,亚铁离子与氢氧根离子反应生成氢氧化亚铁;
B.在酸性溶液中,Al3+、Na+、Cl-、NO3-离子之间不发生反应,也不与氢离子反应;
C.在碱性溶液中,K+、Na+、Cl-、AlO2-离子之间不满足离子反应发生条件,且都不与氢氧根离子反应;
D.酸性溶液中,K+、NH4+、SO42-、NO3-之间不发生反应,都不与氢离子反应.
A.酸性溶液中,亚铁离子和硝酸根离子发生氧化还原反应;碱性溶液中,亚铁离子与氢氧根离子反应生成氢氧化亚铁;
B.在酸性溶液中,Al3+、Na+、Cl-、NO3-离子之间不发生反应,也不与氢离子反应;
C.在碱性溶液中,K+、Na+、Cl-、AlO2-离子之间不满足离子反应发生条件,且都不与氢氧根离子反应;
D.酸性溶液中,K+、NH4+、SO42-、NO3-之间不发生反应,都不与氢离子反应.
解答:
解:由水电离产生的c(OH-)=1×10-15mol/L的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.酸性条件下,Fe2+、NO3-、之间发生氧化还原反应,碱性溶液中,Fe2+与氢氧根离子反应生成氢氧化亚铁,在溶液中一定不能大量共存,故A正确;
B.在酸性溶液中,Al3+、Na+、Cl-、NO3-离子之间不反应,都不与氢离子反应,在溶液中可以大量共存,故B错误;
C.碱性溶液中,K+、Na+、Cl-、AlO2-之间不发生反应,都不与氢氧根离子反应,在溶液中可以大量共存,故C错误;
D.在酸性溶液中,K+、NH4+、SO42-、NO3-之间不发生反应,都不与氢离子反应,在溶液中可以大量共存,故D错误;
故选A.
A.酸性条件下,Fe2+、NO3-、之间发生氧化还原反应,碱性溶液中,Fe2+与氢氧根离子反应生成氢氧化亚铁,在溶液中一定不能大量共存,故A正确;
B.在酸性溶液中,Al3+、Na+、Cl-、NO3-离子之间不反应,都不与氢离子反应,在溶液中可以大量共存,故B错误;
C.碱性溶液中,K+、Na+、Cl-、AlO2-之间不发生反应,都不与氢氧根离子反应,在溶液中可以大量共存,故C错误;
D.在酸性溶液中,K+、NH4+、SO42-、NO3-之间不发生反应,都不与氢离子反应,在溶液中可以大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,为高考中的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
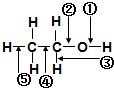

| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、和HBr共热时,键④断裂 |
| D、在铜催化下和氧气反应时,键①和③断裂 |
要想使AlCl3溶液中的Al3+全部沉淀出来,应选用下列试剂中的( )
| A、NaOH溶液 | B、石灰水 |
| C、硫酸 | D、氨水 |
已知一定温度下2X(g)+Y (g)?mZ(g)△H=-a kJ?mol-1 (a>0),现有甲乙两容积相等且固定不变的密闭容器,在保持该温度下,向密闭容器甲中通入2molX和1molY,达到平衡状态时,放出热量bkJ;向密闭容器乙中通入1molX和0.5molY,达到平衡状态时,放出热量ckJ,且b>2c,则a、b、m的值或关系正确的是( )
| A、m=4 | B、a=b |
| C、b<a | D、m等于2或1 |
已知铅蓄电池放电时发生如下反应:负极:Pb+SO42--2e-=PbSO4,正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,当铅蓄电池放电转移的电子能氧化Cl-制得Cl2 22.4L(标况)时,电池内消耗的硫酸的物质的量至少是( )
| A、2.5 mol |
| B、2 mol |
| C、1 mol |
| D、5 mol |
在由水电离出的C[OH-]=1×10-13mol/L的溶液中,能大量共存的离子组是( )
| A、Fe2+ Na+ NO3- Cl- |
| B、Ba2+ Na+ NO3- Cl- |
| C、SO42- SO32- NH4+ Na+ |
| D、Mg2+ Na+ Br- ClO- |
恒温恒压,不做功时,反应A+B═C+D,在下列哪种情况下,一定能自发进行( )
| A、△H<0,△S>0 |
| B、△H>0,△S>0 |
| C、△H<0,△S<0 |
| D、△H>0,△S<0 |
如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )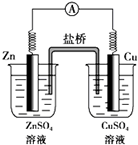

| A、反应中,盐桥中的Cl-会移向ZnSO4溶液 |
| B、取出盐桥后,电流计依然发生偏转 |
| C、铜片上有气泡逸出 |
| D、锌为负极,发生还原反应,电极反应式为:Zn-2e-=Zn2+ |
某温度下,向容积为20L的密闭反应器中充入0.2molHI(g),达到平衡后测得HI的转化率为80%,则该温度下反应H2(g)+I2(g)?2HI(g)的平衡常数是( )
| A、2.5×10-2 |
| B、0.25 |
| C、4.0 |
| D、4.0×102 |