题目内容
现有如下两个反应:
(A)NaOH+HCl═NaCl+H2O
(B)Cu+2Ag+═2Ag+Cu2+
(1)根据两反应本质,判断能否设计成原电池 ;
(2)如果不能,说明其原因 ;
(3)如果可以,则写出正、负极材料及其电极反应时和反应类型(“氧化反应”或“还原反应”):
负极: , , ;
正极: , , ;
若导线上转移电子1mol,则正极质量增加 g,电解质溶液: .
(A)NaOH+HCl═NaCl+H2O
(B)Cu+2Ag+═2Ag+Cu2+
(1)根据两反应本质,判断能否设计成原电池
(2)如果不能,说明其原因
(3)如果可以,则写出正、负极材料及其电极反应时和反应类型(“氧化反应”或“还原反应”):
负极:
正极:
若导线上转移电子1mol,则正极质量增加
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)能设计成原电池的化学反应必须是自发进行的放热的氧化还原反应,否则不能设计成原电池;
(2)非氧化还原反应不能设计成原电池;
(3)根据Cu+2Ag+═2Ag+Cu2+可知Fe应为负极,失电子被氧化,正极可为C、Ag等,正极上Ag+得电子生成Ag,电解质溶液含有Ag+,根据电子守恒计算正极增加的质量.
(2)非氧化还原反应不能设计成原电池;
(3)根据Cu+2Ag+═2Ag+Cu2+可知Fe应为负极,失电子被氧化,正极可为C、Ag等,正极上Ag+得电子生成Ag,电解质溶液含有Ag+,根据电子守恒计算正极增加的质量.
解答:
解:(1)(A)该反应不是氧化还原反应,所以不能设计成原电池,(B)该反应是自发进行的放热的氧化还原反应,所以能设计成原电池,
故答案为:(A)不能,(B)能;
(2)(A)NaOH+HCl═NaCl+H2O该反应中各元素的化合价不变,属于复分解反应,所以不是氧化还原反应,则不能设计成原电池,
故答案为:(A)反应是非氧化还原反应;
(3)Cu+2Ag+=Cu2++2Ag,根据反应前后的金属单质确定电极材料,所以该原电池的电极材料是铜和碳,铜易失去电子发生氧化反应,所以铜作负极,电极反应式为:Cu-2e-=Cu2+,碳作正极发生还原反应,2Ag++2e-=2Ag,若导线上转移电子1mol,则正极增加1molAg,质量为108克,反应物中的化合物为含银离子的可溶性化合物,常见的有硝酸银,所以电解质溶液为硝酸银溶液;
故答案为:铜;Cu-2e-=Cu2+;氧化反应;碳;2Ag++2e-=2Ag;还原反应;108;硝酸银溶液.
故答案为:(A)不能,(B)能;
(2)(A)NaOH+HCl═NaCl+H2O该反应中各元素的化合价不变,属于复分解反应,所以不是氧化还原反应,则不能设计成原电池,
故答案为:(A)反应是非氧化还原反应;
(3)Cu+2Ag+=Cu2++2Ag,根据反应前后的金属单质确定电极材料,所以该原电池的电极材料是铜和碳,铜易失去电子发生氧化反应,所以铜作负极,电极反应式为:Cu-2e-=Cu2+,碳作正极发生还原反应,2Ag++2e-=2Ag,若导线上转移电子1mol,则正极增加1molAg,质量为108克,反应物中的化合物为含银离子的可溶性化合物,常见的有硝酸银,所以电解质溶液为硝酸银溶液;
故答案为:铜;Cu-2e-=Cu2+;氧化反应;碳;2Ag++2e-=2Ag;还原反应;108;硝酸银溶液.
点评:本题考查了原电池的设计和工作原理的探究,为侧重于基础知识的考查,题目难度不大.
注意原电池的设计:
1、基本方法
以氧化还原反应为基础,确定原电池的正负极、电解质溶液及电极反应,可参考锌-铜-稀硫酸原电池模型处理问题.其方法是还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.
2、电解质溶液的选择
电解质溶液一般要能与负极发生反应,或者是电解质溶液中溶解的其它物质与负极发生反应.
3、电极材料的选择
电极材料必须导电,负极必须能够与电解质溶液反应,容易失去电子;正极和负极之间只有产生电势差,电子才能定向运动,所以正极和负极不用同一种材料.
注意原电池的设计:
1、基本方法
以氧化还原反应为基础,确定原电池的正负极、电解质溶液及电极反应,可参考锌-铜-稀硫酸原电池模型处理问题.其方法是还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.
2、电解质溶液的选择
电解质溶液一般要能与负极发生反应,或者是电解质溶液中溶解的其它物质与负极发生反应.
3、电极材料的选择
电极材料必须导电,负极必须能够与电解质溶液反应,容易失去电子;正极和负极之间只有产生电势差,电子才能定向运动,所以正极和负极不用同一种材料.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
如图为正丁腈的结构简式,正丁腈为易燃液体,有毒性,下列有关说法正确的是( )
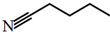

| A、同等条件下,正丁腈在水中的溶解度比在乙醚中的溶解度大 |
| B、其分子式为C4H7N,其密度比水大 |
| C、它还可被命名为氰代丙烷,正丙基氰等,其结构中不含氢键 |
| D、正丁腈由丁烯与氨氧化而得,或由丁醇与氨催化氧化而得 |
 .
.