题目内容
下列物质中,属于强电解质的是( )
| A、CO2 |
| B、HCl |
| C、NH3?H2O |
| D、NaOH溶液 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
解答:
解:A.二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,但二氧化碳自身不能电离,是非电解质,故A错误;
B.HCl在水溶液中完全电离,是强电解质,故B正确;
C.NH3?H2O在水溶液中部分电离,是弱电解质,故C错误;
D.NaOH溶液是混合物,既不是电解质也不是非电解质,故D错误,
故选B.
B.HCl在水溶液中完全电离,是强电解质,故B正确;
C.NH3?H2O在水溶液中部分电离,是弱电解质,故C错误;
D.NaOH溶液是混合物,既不是电解质也不是非电解质,故D错误,
故选B.
点评:本题考查电解质、非电解质、强弱电解质概念的辨析,难度不大.解题时紧抓住强电解质必须是化合物,且在水溶液中是完全电离的.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列物质中,既有离子键又有共价键的是( )
| A、Ca(NO3)2 |
| B、KOH |
| C、H2O |
| D、NH4F |
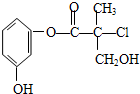 某有机物是药物生产的中间体,其结构简式为下列有关叙述正确的是( )
某有机物是药物生产的中间体,其结构简式为下列有关叙述正确的是( )| A、该有机物与Br2水发生加成反应 |
| B、该有机物与浓硫酸混合加热可发生消去反应 |
| C、该有机物经催化氧化后能发生银镜反应 |
| D、1 mol该有机物与足量NaOH溶液反应最多消耗3 mol NaOH |
CS2(液体)能在氧气中燃烧生成CO2和SO2,将0.228g CS2 在448mL(标况)O2中燃烧,将燃烧后的混合气体恢复到标况时体积为( )
| A、ll2mL |
| B、448mL |
| C、224mL |
| D、336mL |
 在一定条件下,固定容积的密闭容器中反应:2NO2(g)?2NO (g)+O2 (g)△H>0,达到平衡.当改变其中一个条件X,Y随X的变化不符合图中曲线的是( )
在一定条件下,固定容积的密闭容器中反应:2NO2(g)?2NO (g)+O2 (g)△H>0,达到平衡.当改变其中一个条件X,Y随X的变化不符合图中曲线的是( )| A、当X表示温度时,Y表示NO2的物质的量 |
| B、当X表示反应时间时,Y表示混合气体的密度 |
| C、当X表示压强时,Y表示NO2的转化率 |
| D、当X表示NO2的物质的量时,Y表示NO2的转化率 |
 丁香油酚的结构简式如图所示,它不具有的化学性质是( )
丁香油酚的结构简式如图所示,它不具有的化学性质是( )| A、燃烧 |
| B、使酸性高锰酸钾溶液褪色 |
| C、与溴加成 |
| D、与NaHCO3溶液反应放出二氧化碳 |
下列说法正确的是( )
| A、将1 mol NaCl溶于1 L水中,所得溶液的物质的量浓度为1 mol/L |
| B、将2 mol KCl溶于适量水中,配成1L溶液,所得溶液的物质的量浓度为2 mol/L |
| C、将3 mol CuSO4溶于1000 g水中,所得溶液的物质的量浓度为3 mol/L |
| D、将4 mol NaOH溶于适量水中,配成1000 g 溶液,所得溶液的物质的量浓度为4 mol/L |
化学是一门以实验为基础的学科,下列实验操作没有安全隐患的是( )
| A、加热固体时试管口略高于试管底部 |
| B、未经验纯就直接点燃氢气 |
| C、用灯帽盖灭燃着的酒精灯 |
| D、加热后的试管未经冷却就直接用冷水洗涤 |
设nA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、5.6g铁粉与足量水蒸气反应生成的H2分子数为0.10nA |
| B、1mol Mg与足量O2或N2反应生成MgO或Mg3N2失去的电子数为2nA |
| C、46g NO2 和 N2O4混合气体中含有原子数为3nA |
| D、1L 1mol?L-1醋酸溶液中离子总数为2nA |