题目内容
已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):
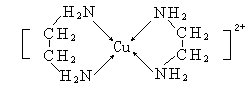
请回答下列问题︰
(1)指出H、O、N三种元素的电负性的大小顺序_______________________。
(2)乙二胺分子中N原子成键时采取的杂化类型是__________________,乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________。
(3)上述配离子中含有的化学键类型有:__________________。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
(4)该配合物[Cu(en)2]Cl2的系统命名为_______;其中铜离子的配位数是___________。
(1)指出H、O、N三种元素的电负性的大小顺序_______________________。
(2)乙二胺分子中N原子成键时采取的杂化类型是__________________,乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________。
(3)上述配离子中含有的化学键类型有:__________________。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
(4)该配合物[Cu(en)2]Cl2的系统命名为_______;其中铜离子的配位数是___________。
(1)O>N>H
(2) sp3;前者存在分子间氢键
(3) a,b,c
(4) 氯化二乙二胺合铜(Ⅱ);4
(2) sp3;前者存在分子间氢键
(3) a,b,c
(4) 氯化二乙二胺合铜(Ⅱ);4

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


