题目内容
(13分) 甲、乙、丙、丁、X是中学阶段的五种常见物质,它们的转化关系如下图所示(部分产物已略去):
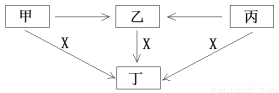
(1)若甲、乙、丙、丁均为化合物,且焰色反应均呈黄色。丙是淡黄色固体,常温下X是一种无色无味气体。则:
①甲和X生成丁的化学方程式为:
②丙和X生成丁的反应中还原剂是 (填化学式),有0.2mol丁生成时,电子转移的数目是 。
(2)若甲、乙、丙、丁都含有地壳中含量最多的金属元素,且丙受热时分解生成乙。X、丁溶液的焰色反应均为紫色(透过蓝色钴玻璃)。
①图中五个转化中属于氧化还原反应的数目是
A.2 B.3 C.4 D.5
②乙和X生成丁的离子方程式为 。
③溶液中生成的丙能够净水,其原因是 。
(1)①Na2O+ CO2== Na2CO3(2分) ②Na2O2 (2分) 0.2NA (2分)
(2)① A(3分) ② Al2O3+2OH—== 2AlO2—+H2O(2分)
③Al(OH)3能凝聚水中的悬浮物(2分)
【解析】
试题分析:(1)甲、乙、丙、丁均为化合物,且火焰均呈黄色,证明含有钠元素,丙是淡黄色固体为Na2O2,X是一种无色无味气体,且丙+X→丁,则X是CO2,丁是Na2CO3,甲+ CO2→Na2CO3,乙+ CO2→Na2CO3,则甲乙可能为Na2O或NaOH,因为甲→乙,所以甲是Na2O,乙是NaOH。①甲和X生成丁的化学方程式为Na2O+ CO2== Na2CO3;②丙和X生成丁的反应为2Na2O2+2CO2===2Na2CO3+O2,Na2O2既是氧化剂又是还原剂。有0.2mol丁生成时,电子转移的数目是0.2NA。(2)地壳中含量最多的金属元素是铝元素,X、丁溶液的焰色反应均为紫色(透过蓝色钴玻璃),则含有钾元素,丙受热分解说明是Al(OH)3,乙是Al2O3,X是KOH,甲是Al。①图中五个转化只有2个属于氧化还原反应,分别是2Al+2KOH=2KAlO2+3H2↑,4Al+3O2= 2Al2O3。②乙和X生成丁的离子方程式为Al2O3+2OH—== 2AlO2—+H2O;③Al(OH)3能凝聚水中的悬浮物。
考点:考查钠铝及其化合物的性质。

 科学实验活动册系列答案
科学实验活动册系列答案下列有关实验操作、现象和结论都正确的是
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入BaCl2溶液,生成白色沉淀 | 证明原溶液一定含SO42- |
B | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑 浊的无色无味气体 | 证明原溶液一定含CO32- |
C | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色 | 证明原溶液中一定不含K+ |
D | 用砂纸打磨过的铝箔在空气中受热熔化,并不滴落 | 证明Al2O3熔点一定高于Al单质 |
 bB (g) 达到平衡后,保持温度不变,将容器体积增加一倍,达到新的平衡时B的浓度是原来的60%,则下列说法不正确的是
bB (g) 达到平衡后,保持温度不变,将容器体积增加一倍,达到新的平衡时B的浓度是原来的60%,则下列说法不正确的是