题目内容
16.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 无色澄清透明溶液中:H+、Cu2+、SO42-、Cl- | |
| B. | 0.1 mol•L-1AlCl3溶液中:H+、Na+、Cl-、SO42- | |
| C. | pH=13的溶液中:NH4+、K+、NO3-、HCO3- | |
| D. | c((OH-)<$\sqrt{{K}_{w}}$的溶液:Ca2+、Fe2+、NO3-、ClO- |
分析 A.Cu2+为蓝色;
B.该组离子之间不反应;
C.pH=13的溶液,显碱性;
D.c((OH-)<$\sqrt{{K}_{w}}$的溶液,显酸性.
解答 解:A.Cu2+为蓝色,与无色不符,故A不选;
B.该组离子之间不反应,可大量共存,故B选;
C.pH=13的溶液,显碱性,不能大量存在NH4+、HCO3-,故C不选;
D.c((OH-)<$\sqrt{{K}_{w}}$的溶液,显酸性,Fe2+分别与NO3-、ClO-发生氧化还原反应,且不能大量存在ClO-,故D不选;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
6. 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )| A. | a 电极发生反应:H2NCH2CH2NH2+16e-+4H2O═2CO2↑+N2↑+16H+ | |
| B. | 质子交换膜处H+由右向左移动 | |
| C. | 该电池在微生物作用下将化学能转化为电能 | |
| D. | 开始放电时b极附近pH不变 |
4.下列有关物质的性质和用途的描述均正确的是( )
| A. | 二氧化锰具有强氧化性.能将双氧水氧化为氧气 | |
| B. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| C. | 炭具有还原性,可用炭在高温下将二氧化硅还原为硅 | |
| D. | 汽油是常见的有机溶剂,可以用裂化汽油来萃取溴水中的溴 |
1.下列指定反应的离子方程式正确的是( )
| A. | 用白醋除铁锈:Fe2O3•xH2O+6H+═(3+x)H2O+2Fe3+ | |
| B. | 用惰性电极电解 MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向NH4Al(SO4)2溶液中加入过量的 NaOH溶液:Al3++4OH-═AlO2-+2H2O | |
| D. | 向含NH3的污水中加入NaClO将其转化为N2:3ClO-+2NH3═3Cl-+N2↑+3H2O |
8.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含有大量Fe3+的溶液中:Na+、Fe2+、Br-、SO42- | |
| B. | 1.0 mol/L KMnO4的溶液中:H+、Na+、Cl-、SO42- | |
| C. | 能与铝反应放出H2的溶液中:K+、Mg2+、SO42-、NO3- | |
| D. | 水电离的c(H+)和C(OH-)之积为l×l0-20mol2•L-2的溶液中:Na+、K+、CO32-、Cl- |
16.下列各种物质在一定条件下反应,所得产物种类与反应物的用量或条件无关的是( )
| A. | Ca(HCO3)2溶液与Ca(OH)2反应 | B. | Fe 与 O2反应 | ||
| C. | NaAlO2溶液与CO2反应 | D. | NH4HCO3溶液与NaOH反应 |
17.下列将饱和碘水中的碘单质分离出来的实验操作说法正确的是( )
| A. | 使用萃取的方法,并选用酒精作萃取剂 | |
| B. | 萃取使用的主要仪器是分液漏斗,在使用前要先检验其是否漏液 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一烧杯中 | |
| D. | 从分液漏斗中分离出的就是纯净的碘单质 |
 .G的结构简式为
.G的结构简式为 .
. +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaCl.
+2NaCl.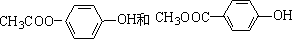 .
.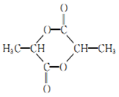 的合成路线:
的合成路线: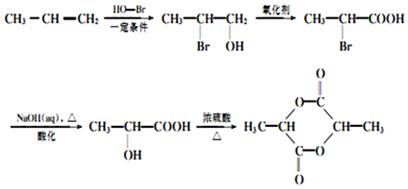 .
.