题目内容
13.高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH $\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O;K2MnO4歧化:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3.
已知K2MnO4溶液显绿色.请回答下列问题:
(1)MnO2熔融氧化应放在④中加热(填仪器编号).
①烧杯 ②瓷坩埚 ③蒸发皿 ④铁坩埚
(2)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行,A、B、C、D、E为旋塞,F、G为气囊,H为带套管的玻璃棒.
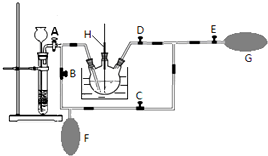
①为了能充分利用CO2,装置中使用了两个气囊.当试管内依次加入块状碳酸钙和盐酸后,关闭旋塞B、E,微开旋塞A,打开旋塞C、D,往热K2MnO4溶液中通入CO2气体,未反应的CO2被收集到气囊F中.待气囊F收集到较多气体时,关闭旋塞A、C,打开旋塞B、D、E,轻轻挤压气囊F,使CO2气体缓缓地压入K2MnO4溶液中再次反应,未反应的CO2气体又被收集在气囊G中.然后将气囊G中的气体挤压入气囊F中,如此反复,直至K2MnO4完全反应.
②检验K2MnO4歧化完全的实验操作是用玻璃棒蘸取三颈烧瓶内的溶液点在滤纸上,若滤纸上只有紫红色痕迹,无绿色痕迹,表明反应已歧化完全.
(3)将三颈烧瓶中所得产物进行抽滤,将滤液倒入蒸发皿中,蒸发浓缩至溶液表面出现晶膜为止,自然冷却结晶,抽滤,得到针状的高锰酸钾晶体.本实验应采用低温烘干的方法来干燥产品,原因是高锰酸钾晶体受热易分解.
(4)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O
现称取制得的高锰酸钾产品7.245g,配成500mL溶液,用移液管量取25.00mL待测液,用0.1000mol•L-1草酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.00mL(不考虑杂质的反应),则高锰酸钾产品的纯度为87.23%(保留4位有效数字,已知M(KMnO4)=158g•mol-1).若移液管用蒸馏水洗净后没有用待测液润洗或烘干,则测定结果将偏小.(填“偏大”、“偏小”、“不变”)
分析 (1)熔融固体物质需要在坩埚内加热,加热熔融物含有碱性KOH应用铁坩埚;
(2)①该操作的目的是将气囊F中的二氧化碳排出,据此判断正确的操作方法;
②根据“K2MnO4溶液显绿色”可知,如果该歧化反应结束,则反应后的溶液不会显示绿色;
(3)蒸发溶液获得晶体时不能蒸干,避免固体飞溅;高锰酸钾在温度较高时容易分解,需要低温下烘干;
(4)根据n=cV计算出25mL待测液消耗的醋酸钠的物质的量,再根据反应方程式计算出25mL待测液中含有高锰酸钾的物质的量,从而计算出样品中含有高锰酸钾的物质的量,然后根据m=nM计算出高锰酸钾的质量,最后计算出纯度;待测液被蒸馏水稀释后浓度减小,测定的样品中含有的高锰酸钾物质的量减小,纯度减小.
解答 解:(1)熔融固体物质需要在坩埚内加热,加热熔融物中含有碱性KOH,瓷坩埚中含有二氧化硅,二氧化硅能够与氢氧化钾反应,所以应用铁坩埚,所以④正确,
故答案为:④;
(2)①待气囊F收集到较多气体时,需要将气囊F中二氧化碳排出到热K2MnO4溶液中,所以需要关闭A、C,打开B、D、E,轻轻挤压气囊F,从而使CO2气体缓缓地压入K2MnO4溶液中再次反应,
故答案为:A、C;B、D、E;
②由于K2MnO4溶液显绿色,所以用玻璃棒蘸取三颈烧瓶内的溶液点在滤纸上,若滤纸上只有紫红色痕迹,无绿色痕迹,表明反应已歧化完全,
故答案为:用玻璃棒蘸取三颈烧瓶内的溶液点在滤纸上,若滤纸上只有紫红色痕迹,无绿色痕迹,表明反应已歧化完全;
(3)蒸发溶液获得高锰酸钾时不能蒸干,避免固体飞溅及高锰酸钾的分解,所以应该加热到溶液表面出现晶膜时停止加热,并且应采用低温烘干的方法来干燥产品,避免高锰酸钾晶体受热发生分解,
故答案为:溶液表面出现晶膜为止;高锰酸钾晶体受热易分解;
(4)50mL 0.1000mol•L-1草酸钠标准溶液中含有醋酸钠的物质的量为:0.1mol/L×0.05L=0.005mol,根据反应2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O可知,消耗0.005mol醋酸钠需要消耗高锰酸根离子的物质的量为:0.005mol×$\frac{5}{2}$=0.002mol,
500mL配制的样品溶液中含有高锰酸根离子的物质的量为:0.002mol×$\frac{500mL}{25mL}$=0.04mol,
则样品中含有高锰酸钾的质量为:0.04mol×158g•mol-1=6.32g,
则高锰酸钾产品的纯度为:$\frac{6.32g}{7.245g}$×100%=87.23%;
若移液管用蒸馏水洗净后没有用待测液润洗或烘干,则导致待测液浓度减小,滴定时消耗的标准液体积偏小,测定结果偏小,
故答案为:87.23%;偏小.
点评 本题通过高锰酸钾的制备,考查了物质制备实验方案的设计方法,题目难度中等,涉及了样品中纯度计算、化学实验基本操作方法、物质制备原理等知识,明确物质制备原理及流程为解答本题的关键,试题充分考查了学生的分析、理解能力及化学实验、化学计算的能力.

| A. | 加5 mL水,c (H+)增大 | B. | 加少量NaCl固体,c (H+)不变 | ||
| C. | 加少量碳酸钙粉末,c(HClO)升高 | D. | 加少量Na2SO3固体,溶液pH升高 |
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是BaSO4.
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2.
①支持甲同学观点的实验证据是液面上方略显浅棕色.
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+.
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
向2mL0.1mol/LBaCl2 溶液(填化学式)中通入SO2 | 试管内有白色沉淀产生 |
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | 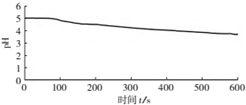 图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线. | 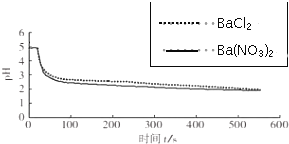 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
(4)图2,BaCl2溶液中发生反应的离子方程式为2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+.
(5)依据上述图象你得出的结论是在氧化SO2的过程中,O2起了主要作用,说明理由在BaCl2溶液中起氧化作用的是O2,在Ba(NO3)2溶液中起氧化作用的是O2和NO3-,而图2中,分别向BaCl2、Ba(NO3)2溶液中通入SO2,pH变化趋势、幅度接近,因此起氧化作用的主要是O2.
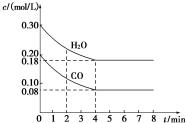 在一体积为1L的密闭容器中,通入一定量的CO和H2O,在T1℃时发生如下反应:CO (g)+H2O(g)?CO2(g)+H2(g)△H<O,CO和H2O浓度变化如图,则
在一体积为1L的密闭容器中,通入一定量的CO和H2O,在T1℃时发生如下反应:CO (g)+H2O(g)?CO2(g)+H2(g)△H<O,CO和H2O浓度变化如图,则(1)0~4min CO的平均反应速率v(CO)=0.03mol/(L.min).
(2)达平衡时CO的转化率为60%,T1℃时该反应的平衡常数K=1.
(3)T2℃(高于T1℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | C4 |
②4~5min时,平衡向逆反应方向移动,可能的原因是d(填字母).
a.增加水蒸气 b.降低温度
c.增大了CO2浓度 d.增加了氢气浓度.
| A. | 1 mol强酸和1 mol强碱完全反应所放出的热量称为中和热 | |
| B. | 热化学方程式中表明的热量是指每摩尔反应物反应时吸收或放出的热量 | |
| C. | 1 mol碳燃烧所放出的热量为燃烧热 | |
| D. | 热化学方程式中的化学计量数表示物质的量,因此可用分数表示 |
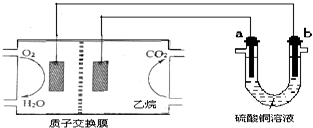
| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | a极是铜,b极是铁时,硫酸铜溶液浓度减小 | |
| C. | a、b两极若是石墨,在同温同压下a极产生的气体与电池中消耗的乙烷体积的7/2 | |
| D. | a极是纯铜,b极是粗铜时,a极上有铜析出,b极逐渐溶解,两极质量变化相同 |
| A. | 原子半径C>D>E | |
| B. | A2E6分子中各原子均满足8电子结构 | |
| C. | 气态氢化物的稳定性HmE>HnD | |
| D. | B、C形成的化合物中只可能存在离子键 |
②N2(g)+3H2 (g)?2NH3 (g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
| A. | 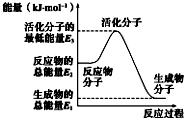 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和 3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和 6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | |
| D. | 氨的催化氧化反应为 4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol-1 |