题目内容
12.下列反应中氯元素全部被还原的是( )| A. | 5Cl2+I2+6H2O=10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | |
| C. | MnO2+4HCl=MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$ 2NaOH+Cl2↑+H2↑ |
分析 反应中氯元素全部被还原,Cl元素的化合价应降低,含有Cl元素的物质在反应中表现为氧化性,以此解答该题.
解答 解:A.反应中Cl元素化合价全部降低,被还原,则反应中氯元素全部被还原,故A正确;
B.反应中Cl元素化合价既升高又降低,既被氧化又被还原,故B错误;
C.反应中Cl化合价部分升高,被氧化,部分表现为酸性,故C错误;
D.反应中Cl化合价全部升高,被氧化,故D错误.
故选A.
点评 本题考查氧化还原反应,注意从元素化合价变化的角度认识物质表现出的性质,题目难度不大.

练习册系列答案
相关题目
19.下列有关纯碱和小苏打的叙述中正确的是( )
| A. | Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠溶液反应 | |
| B. | 等质量Na2CO3、NaHCO3分别与相同浓度的盐酸反应,NaHCO3消耗的盐酸体积少 | |
| C. | 向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 | |
| D. | 等物质的量Na2CO3、NaHCO3分别与足量稀H2SO4反应,NaHCO3产生的CO2多 |
16.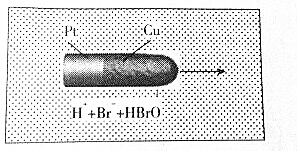 世界上最小的纳米发动机比盐粒小500倍,它由微型铜箔电池供电,放入Br2的稀溶液中(Br2+H2O=H++Br-+HBrO)铜铂电池开始工作,整个纳米发动机会朝着铜电极所指的方向运动,如下图所示.下列说法正确的是( )
世界上最小的纳米发动机比盐粒小500倍,它由微型铜箔电池供电,放入Br2的稀溶液中(Br2+H2O=H++Br-+HBrO)铜铂电池开始工作,整个纳米发动机会朝着铜电极所指的方向运动,如下图所示.下列说法正确的是( )
 世界上最小的纳米发动机比盐粒小500倍,它由微型铜箔电池供电,放入Br2的稀溶液中(Br2+H2O=H++Br-+HBrO)铜铂电池开始工作,整个纳米发动机会朝着铜电极所指的方向运动,如下图所示.下列说法正确的是( )
世界上最小的纳米发动机比盐粒小500倍,它由微型铜箔电池供电,放入Br2的稀溶液中(Br2+H2O=H++Br-+HBrO)铜铂电池开始工作,整个纳米发动机会朝着铜电极所指的方向运动,如下图所示.下列说法正确的是( )| A. | 铂电极未电池的负极 | |
| B. | 铜电极表面有气泡产生 | |
| C. | 铂电极的电极反应式为HBrO+H++2e-=Br-+H2O | |
| D. | 电池工作时实现机械能→电能→化学能的转化 |
7.下列各装置,能构成原电池的是( )
| A. | 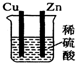 | B. | 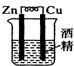 | C. | 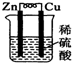 | D. |  |
17.由于合金的说法不正确的是( )
| A. | 合金是由两种金属或两种非金属熔合而成的物质 | |
| B. | 合金的硬度较大,多数的合金的熔点比各成分的金属的低 | |
| C. | 根据所添加的元素的种类、含量来调节合金的性能 | |
| D. | 不锈钢在大气中比较稳定,不容易生锈,具有很强的抗腐蚀能力 |
4.下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去KCl中的MnO2 | 蒸发结晶 | 溶解度不同 |
| B | 除去碘中的NaCl | 加热、升华 | NaCl的熔点高,碘易升华 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
1.在海轮的船壳上连接锌块,下列相关说法正确的是( )
| A. | 制成合金保护船体 | B. | 锌块的反应:Zn-2e→Zn2 | ||
| C. | 船体的反应:Fe-2e→Fe2+ | D. | 是外加电流的阴极保护法 |