题目内容
图5-7是一个实验室测定黄铁矿中硫的质量分数的装置图。实验时有如下操作: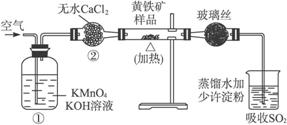
图5-7
A.将磁管中样品加热到800~850 ℃
B.称取研细的黄铁矿样品
C.连接全部仪器,使其成为整套实验装置,并检查气密性
D.将样品小心放入容器中,再将容器小心地推入磁管中部
E.以每分钟1 L的速度鼓入空气
F.用标准碘液滴定含淀粉的SO2水溶液
(1)正确的实验步骤,其操作编号是_______________。
(2)装置①的作用是______________________;装置②的作用是__________________。
(3)应根据____________现象判断滴定已达到终点而停止鼓入空气。
(4)碘液跟二氧化硫水溶液发生反应的化学方程式是_________________。
(5)假定矿样品的硫全部转化为二氧化硫,并全部被水吸收。若称得矿样的质量是0.12 g,滴定管中碘液初读数为0.10 mL,末读数为25.60 mL,标准碘液的浓度为0.050 mol·L-1,则黄铁矿样品中硫的质量分数是__________。(列式及答案)
解析:V〔I2(aq)〕=25.60 mL-0.10 mL=25.50 mL,
n(I2)=c(I2)·V〔I2(aq)〕=0.050 mol·L-1×25.50×10-3L=1.275×10-3mol
根据I2+SO2+2H2O====H2SO4+2HI可知n(S)=n(SO2)=n(I2)
w(S)=m(S)/m(矿样)×100%=(1.275×10-3mol×32 g·mol-1)/0.12 g×100%=34%。
答案: (1)CBDEAF
(2)除去空气中的CO2和还原性气体,净化空气 吸收水蒸气,干燥空气
(3)向吸收SO2的液体中滴加一滴碘液后,溶液变为蓝色,且在半分钟内不褪色
(4)I2+SO2+2H2O====H2SO4+2HI
(5)![]() ×100%=34%
×100%=34%

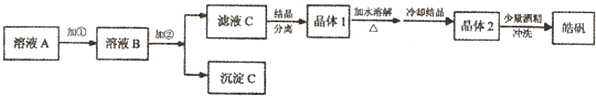
 (2011?浙江)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(2011?浙江)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
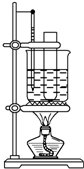 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示: