题目内容
0.1 mol Al2(SO4)3中含有Al3+ mol、SO42- 个.
考点:物质的量的相关计算
专题:
分析:根据Al2(SO4)3的电离方程式确定Al2(SO4)3中含有离子的物质的量..
解答:
解:Al2(SO4)3=2Al3++3SO42-,0.1molAl2(SO4)3溶液,Al3+物质的量n=0.1mol×2=0.2mol/L,SO42-物质的量n=0.1mol×3=0.3mol,个数为:N=n×NA=0.3NA=1.806×1023,
故答案为:0.2; 0.3 NA(或1.806×1023).
故答案为:0.2; 0.3 NA(或1.806×1023).
点评:本题考查了Al2(SO4)3中离子的物质的量计算,掌握硫酸铝的构成与离子间的关系是解答关键,题目较简单.

练习册系列答案
相关题目
在标准状况下,1.12L的某气态单质质量为2.4克,若组成此单质的元素相对原子质量为16,则此单质的相对分子质量及一个分子中含该原子的个数为( )
| A、16和1 | B、32和2 |
| C、48和3 | D、64和4 |
在浩瀚的大海里蕴藏着丰富的化学资源.海水的综合利用是当前非常重要的一个课题.下列有关说法正确的是( )
| A、海水中含量最高的是Na元素和Cl元素 | ||||||
| B、海水晒盐的原理与化学实验中的蒸发操作相似 | ||||||
| C、为了消除碘缺乏病,我国政府规定在食盐中必须加入一定量的I2 | ||||||
D、海水提镁可以通过以下步骤进行:海水
|
某实验需要470mL0.4mol?L-1NaOH溶液,配制该溶液时,用托盘天平称取NaOH固体的质量应为( )
| A、8.0g | B、7.5g |
| C、4.0g | D、7.52g |
关于溶液的酸性强弱的说法中,正确的是( )
| A、只要溶液里有H+,溶液就显酸性 |
| B、H+浓度增大,溶液的酸性一定增强 |
| C、c(H+)>c(OH-),溶液一定显酸性 |
| D、强酸溶液的酸性一定比弱酸溶液的酸性强 |
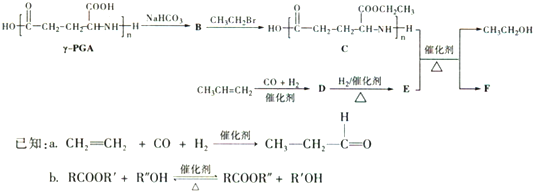
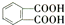 )反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有
)反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有 请按下列要求填空
请按下列要求填空