题目内容
下列关于氯及其化合物的说法正确的是( )
| A、钠在Cl2中燃烧,产生大量黄烟 |
| B、HClO是弱酸,所以NaCIO是弱电解质 |
| C、Cl2通入H2S饱和溶液中出现浑浊,说明氧化性:Cl2>S |
| D、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
考点:钠的化学性质,氯气的化学性质,氯、溴、碘及其化合物的综合应用
专题:
分析:A.钠在Cl2中燃烧,产生大量白烟;
B.HClO是弱电解质,但NaClO是强电解质;
C.氯气通入H2S饱和溶液中出现浑浊,说明氯气置换出硫;
D.新制氯水含有HClO,具有漂白性.
B.HClO是弱电解质,但NaClO是强电解质;
C.氯气通入H2S饱和溶液中出现浑浊,说明氯气置换出硫;
D.新制氯水含有HClO,具有漂白性.
解答:
解:A.钠在Cl2中燃烧生成白色的氯化钠固体小颗粒,所以产生大量白烟,故A错误;
B.HClO是弱电解质,但NaClO在水溶液里或熔融状态下完全电离,所以NaClO属于强电解质,故B错误;
C.氯气通入H2S饱和溶液中出现浑浊,说明氯气置换出硫,发生Cl2+H2S=2HCl+S↓,可说明氧化性:Cl2>S,故C正确;
D.新制氯水含有HClO,具有漂白性,向其中滴加少量紫色石蕊试液,溶液先变红后褪色,故D错误.
故选C.
B.HClO是弱电解质,但NaClO在水溶液里或熔融状态下完全电离,所以NaClO属于强电解质,故B错误;
C.氯气通入H2S饱和溶液中出现浑浊,说明氯气置换出硫,发生Cl2+H2S=2HCl+S↓,可说明氧化性:Cl2>S,故C正确;
D.新制氯水含有HClO,具有漂白性,向其中滴加少量紫色石蕊试液,溶液先变红后褪色,故D错误.
故选C.
点评:本题考查氯气的性质,侧重于元素化合物知识的综合考查和应用,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
绿原酸的结构简式如图,下列有关绿原酸的说法正确的是( )
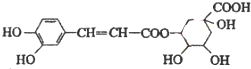
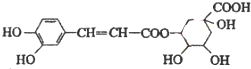
| A、分子式为C16H15O9 |
| B、不能与NaHCO3溶液反应 |
| C、能发生取代反应和消去反应 |
| D、1 mol绿原酸最多与可8mol NaOH反应 |
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,有CO32-或HCO3-中的一种或两种 |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
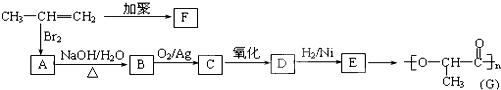
 (Ⅰ)乙苯的结构简式可以表示为
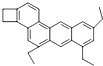
(Ⅰ)乙苯的结构简式可以表示为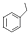 ,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.
,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.