题目内容
已知混合溶液中Na2CO3 和NaHCO3 都为1mol,那么溶液中离子大小排列顺序关系是 .
考点:离子浓度大小的比较
专题:
分析:混合溶液中Na2CO3 和NaHCO3 都为1mol,溶液体积相等,则二者的物质的量浓度相等,CO32-、HCO3-都水解导致溶液呈碱性,且CO32-的水解程度大于HCO3-,HCO3-水解程度大于电离程度,据此判断溶液中离子浓度大小顺序.
解答:
解:混合溶液中Na2CO3 和NaHCO3 都为1mol,溶液体积相等,则二者的物质的量浓度相等,CO32-、HCO3-都水解导致溶液呈碱性,所以c(OH-)>c(H+),且CO32-的水解程度大于HCO3-,所以c(HCO3-)>c(CO32-),HCO3-水解程度大于电离程度,根据物料守恒得c(Na+)>c(HCO3-),盐类水解程度较小,所以c(CO32-)>c(OH-),则该混合溶液中离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
点评:本题考查离子浓度大小比较,为高考高频点,明确溶液中溶质性质是解本题关键,注意多元弱酸根离子水解程度相对大小,会根据电荷守恒、物料守恒解答,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
无土栽培中,需配制一种含 50mol NH4Cl、16mol KCl 和24mol K2SO4的营养液.若用 KCl、NH4Cl 和 (NH4)2SO4 三种固体为原料来配制,其物质的量分别为( )
| A、2 mol、64 mol、24 mol |
| B、64 mol、2 mol、24 mol |
| C、32 mol、50 mol、12 mol |
| D、16 mol、50 mol、24 mol |
咖啡酸可用作化学原料的中间体,其结构如图.下列关于咖啡酸的说法中正确的是( )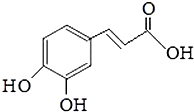

| A、分子中所有官能团均能与NaOH反应,且反应原因相同 |
| B、一定条件下,咖啡酸能够发生取代反应、加聚反应、缩聚反应,但不能与NaHCO3溶液反应 |
| C、分子中的所有碳原子可能共平面,但氧原子不可能与所有碳原子处于同一平面上 |
| D、咖啡酸与浓溴水反应,一个咖啡酸分子中最多能引入5个溴原子 |
下列实验操作中错误的是( )
| A、萃取操作时,所选萃取剂必须与原溶剂互不相溶 |
| B、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
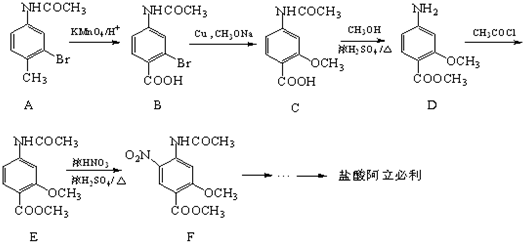
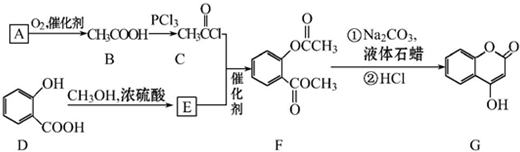
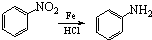 .请写出以
.请写出以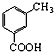 、CH3CH2CH2COCl、CH3OH为原料制备
、CH3CH2CH2COCl、CH3OH为原料制备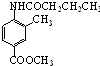 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图: .
.
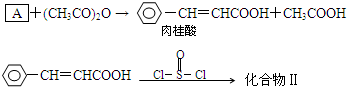
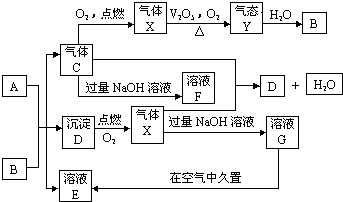
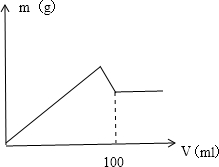 有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.
有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.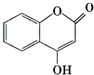 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: