题目内容
17.某兴趣小组用如图装置探究氨的催化氧化反应原理.查阅资料得知:2NaOH+NO+NO2═2NaNO2+H2O
2NaOH+2NO2═NaNO3+NaNO3+H2O
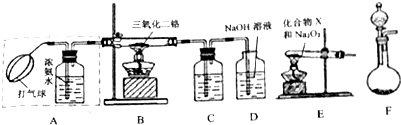
(1)写出实验室制NH3的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,若用装置F制备NH3,可选用的试剂是浓氨水和NaOH固体(或生石灰或碱石灰等)(填名称)
(2)氨催化氧化的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O
(3)加热玻璃管B一段时间后,挤压A中打气球鼓入空气,观察到B中物质呈红热状态;停止加热后仍能保持红热,该反应是放热反应(填“吸热”或“放热”).
(4)为保证在装置C液面上方观察到红棕色气体,装置C盛放的试剂是浓H2SO4;装置D的作用是吸收剩余的氮氧化物防止污染环境.
(5)为实现氨的催化氧化,也可用装置E替换装置A(填装置代号);化合物X为NH4Cl(只写一种),Na2O2的作用是与HCl反应生成氧气.
分析 (1)实验室用固体氯化铵和熟石灰粉末混合加热制取氨气;用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气;
(2)氨气具有还原性,在催化剂作用下可与氧气反应被氧化为NO;
(3)根据反应现象判断,停止加热后仍能保持红热,即可说明该反应放热;
(4)红棕色气体为NO2,易与水反应,应干燥,氮氧化物为污染性气体不能排放到空气中;
(5)装置1能提供氨气和氧气,装置5也能提供氨气和氧气,但装置5中应加入氯化铵和过氧化钠,可生成氨气和氧气.
解答 解:(1)实验室用氯化铵和消石灰反应生成氨气和氯化钙、水,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;F装置是固体和液体不加热制备气体,用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;浓氨水和NaOH固体(或生石灰或碱石灰等);
(2)氨气具有还原性,在催化剂作用下可与氧气反应被氧化为NO,反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)停止加热后仍能保持红热,即可说明该反应放热,故答案为:放热;
(4)NO2易与水反应,为保证在装置C液面上方观察到红棕色气体,应用浓硫酸干燥,装置D的作用是吸收剩余的氮氧化物防止污染环境,
故答案为:浓H2SO4;吸收剩余的氮氧化物防止污染环境;
(5)装置A能提供氨气和氧气,装置E也能提供氨气和氧气,但装置E中应加入氯化铵和过氧化钠,可生成氨气和氧气,反应为:NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$HCl+NH3,2HCl+Na2O2═2NaCl+O2+H2O.
故答案为:A; NH4Cl;与HCl反应生成氧气.
点评 本题考查氨气的制取原理、反应装置及化学性质,题目较为综合,涉及氨气的制取、性质以及二氧化氮和硝酸铵等知识,注意把握元素化合物知识的理解和应用,难度中等.

| A. | 含0.1molHCl溶液中含氢元素0.1NA | |
| B. | 22.4 L 水蒸气含原子数为3NA | |
| C. | 3.4g H2O2中含有的共用电子对数为0.1 NA | |
| D. | 标准状况下,1mol辛烷含有的氢原子数为18NA |
| A. | Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强 | |
| B. | 自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 | |
| C. | 工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质 | |
| D. | 钠与氧气反应的产物与反应条件无关 |
| A. | 二氧化硫常用于食品漂白 | |
| B. | 碳酸氢钠常用于焙制糕点 | |
| C. | 氢氧化铝可作耐高温材料 | |
| D. | 氧化钠常用作呼吸面具中的氧气来源 |
| A. | 与足量酸反应:离子方程式相同 | |
| B. | 热稳定性:Na2CO3<NaHCO3 | |
| C. | 常温下在水中的溶解度:Na2CO3>NaHCO3 | |
| D. | 等物质的量与足量酸反应产生CO2的质量:Na2CO3<NaHCO3 |
| A. | MgCl2 | B. | NH4C1 | C. | CO 2 | D. | NaOH |
| A. | 只有第ⅡA族元素的原子最外层有2个电子 | |
| B. | L电子层为奇数的所有元素都是非金属 | |
| C. | 第三、四、五、六周期元素的数目分别是18、18、32、32 | |
| D. | 由左至右第8、9、10三列元素中没有非金属元素 |
| A. | 电子转移的物质的量为1mol | |
| B. | 断裂了1mol C-H键,转移的电子数目为2NA | |
| C. | 有4gCH4参加反应,生成了5.6L的CO2 | |
| D. | 1mol CH4 (g)和2molO2(g)的能量总和大于1mol CO2 (g)和2molH2O的能量总和 |
| A. | 银镜反应 | B. | 制备硝基苯 | ||
| C. | 皂化反应 | D. | 检验卤代烃中的卤原子 |