题目内容
已知热化学方程式2H2(g)+O2(g)=2H2O(l)△H1<0;2H2O(g)=2H2(g)+O2(g)△H2.下列说法正确的是( )
| A、方程式中化学计量数表示分子数 |
| B、△H2>0 |
| C、△H2=-△H1 |
| D、利用△H1,△H2可求出水的气化热 |
考点:反应热和焓变,化学平衡建立的过程
专题:化学反应中的能量变化
分析:A、热化学方程式中计量数只表示物质的量;
B、水分解反应是吸热反应;
C、反应中水的状态不同,反应焓变数值不同;
D、依据盖斯定律和热化学方程式计算得到水蒸气变化为液态水的能量变化.
B、水分解反应是吸热反应;
C、反应中水的状态不同,反应焓变数值不同;
D、依据盖斯定律和热化学方程式计算得到水蒸气变化为液态水的能量变化.
解答:
解:A、热化学方程式中计量数只表示物质的量,不表示微粒数,可以用分数表示,故A错误;
B、水分解反应是吸热反应,△H2>0,故B正确;
C、反应中水的状态不同,反应焓变数值不同,故C错误;
D、依据盖斯定律和热化学方程式计算得到水蒸气变化为液态水的能量变化,
①2H2(g)+O2(g)=2H2O(l)△H1<0;
②2H2O(g)=2H2(g)+O2(g)△H2;
盖斯定律①+②得到H2O(g)=H2O(l)△H=
KJ/mol,故D正确;
故选BD.
B、水分解反应是吸热反应,△H2>0,故B正确;
C、反应中水的状态不同,反应焓变数值不同,故C错误;
D、依据盖斯定律和热化学方程式计算得到水蒸气变化为液态水的能量变化,
①2H2(g)+O2(g)=2H2O(l)△H1<0;
②2H2O(g)=2H2(g)+O2(g)△H2;
盖斯定律①+②得到H2O(g)=H2O(l)△H=
| △H1+△H2 |
| 2 |
故选BD.
点评:本题考查了热化学方程式的意义,盖斯定律计算分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再向过滤中加入适量的盐酸,这种试剂是( )
| A、NH3.H2O |
| B、NaOH |
| C、Na2CO3 |
| D、MgCO3 |
下列化合物中既存在离子键,又存在配位键的是( )
| A、H2O |
| B、NH4Cl |
| C、NaOH |
| D、Na2O2 |
以下表述不符合元素周期律观点的是( )
| A、酸性:H3PO4>HNO3>HClO4 |
| B、稳定性:HF>H2O>NH3 |
| C、微粒半径:F->Na+>Mg2+ |
| D、碱性:KOH>NaOH>Mg(OH)2 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如下图为N2(g)相 O2(g)反应生成NO(g)过程中的能量变化:下列说法正确的是( )
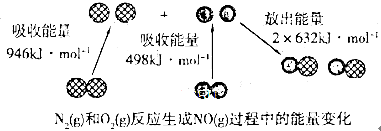

| A、1mol N2(g)和1molO2(g)具有的总能量大于 2mol NO(g)具有的总能量 |
| B、1molN2(g)和lmolO2(g)反应生成2molNO(g)吸收180 kJ热量 |
| C、通常情况下N2(g)和O2(g)混合能直接反应生成NO |
| D、数据不足,不能确定反应热的大小 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、铁发生氧化还原反应,一定失去NA个电子 |
| B、18gD2O含有的质子数为10NA |
| C、常温常压下,46gNO2和N2O4的混合物中含有的原子数为3NA |
| D、1mol/LNa2CO3溶液中含有的Na+数目为2NA |