题目内容
9.为测定某有机化合物A的结构,进行如下实验:(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质中各元素的原子个数比是2:6:1.
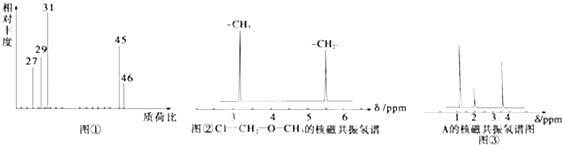
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,该物质的分子式是C2H6O.
(3)根据价键理论,预测A的可能结构并写出结构简式CH3CH2OH、CH3OCH3.
(二)结构式的确定:
(4)核磁共振氢谱能对有机物分子中不同化学环境的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(ClCH2OCH3)有两种氢原子如图②.经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为CH3CH2OH.
(三)性质实验:
(5)A在一定条件下可以和金属钠反应,书写化学方程式:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑.
(6)A在一定条件下可以和乙酸发生酯化反应生成乙酸乙酯,书写化学方程式:CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
分析 (1)根据元素守恒可判断有机化合物中一定含有C和H两种元素,根据生成8.8g的二氧化碳中C元素质量即为化合物中所含C元素质量、生成5.4g 的水中H元素质量即为化合物中所含H元素质量,对氧元素的确定要根据二氧化碳和水中的氧元素质量之和与氧气中氧元素的质量来分析,若前者大,则有机化合物有氧元素,两者相等,则有机化合物没有有氧元素,然后求出各自的物质的量,根据各元素的物质的量之比可推测实验式(最简式);
(2)根据图①所示质谱图判断有机物A的相对分子量,再根据(1)的计算结果判断有机物A的分子式;
(3)根据分子式及书写同分异构体的方法写出A可能的同分异构体的结构简式;
(4)核磁共振氢谱图中含有几个峰,表示该有机物中含有几个位置不同的氢原子,据此判断有机物A的结构;
(5)A在一定条件下可以和金属钠反应,说明A为乙醇,书写乙醇与钠反应的方程式;
(6)A在一定条件下可以和乙酸发生酯化反应生成乙酸乙酯,说明A为乙醇,书写乙醇与乙酸反应的方程式.
解答 解:(1)根据质量守恒定律得:化合物中所含C元素质量为:8.8g×$\frac{12}{44}$=2.4g,所含H元素质量为:5.4g×$\frac{2}{18}$=0.6g,二氧化碳和水中的氧元素质量之和为(8.8g-2.4g)+(5.4g-0.6g)=11.2g,而氧气的质量为$\frac{6.72L}{22.4L/mol}$×32g/mol=9.6g,所以有机物中氧元素质量为11.2g-9.6g=1.6g,
n(C):n(H):n(O)=$\frac{2.4}{12}$:$\frac{0.6}{1}$:$\frac{1.6}{16}$=2:6:1,所以化合物的实验式(最简式)是C2H6O;
故答案为:2:6:1;
(2)据(1)可知,该有机物A的实验式为C2H6O,设该有机物的分子式为(C2H6O)m,由图①质谱图知,最大的质荷比为46,则其相对分子质量为46,则:46m=46,解得:m=1,故其分子式为C2H6O,
故答案为:C2H6O;
(3)A的分子式为C2H6O,A为饱和化合物,有机物A的结构为:CH3CH2OH或CH3OCH3,
故答案为:CH3CH2OH、CH3OCH3;
(4)根据图③A的核磁共振氢谱图可知:A有三种不同类型的H原子,而CH3OCH3只有一种类型的H原子,故A的结构简式为CH3CH2OH,
故答案为:CH3CH2OH;
(5)乙醇能和钠发生反应生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(6)乙酸与乙醇发生酯化反应生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,故答案为:CH3COOH+HOC2H5$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
点评 本题考查了有机物的分子式、结构简式确定以及性质,题目难度中等,注意掌握确定有机物分子式、结构简式的方法,明确质谱仪中的质荷比、核磁共振氢谱中峰的含义为解答本题的关键.


| A. | 分子式为C10H8O6 | |
| B. | 分子中含有3种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3mol NaOH发生中和反应 |
| A. | 烷烃分子中碳原子不可能在同一平面上 | |
| B. | 烷烃易被酸性高锰酸钾溶液氧化 | |
| C. | 在光照条件下,烷烃易与溴水发生取代反应 | |
| D. | 烷烃的卤代反应很难得到纯净的产物 |
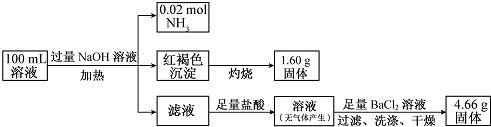
由此可推测原溶液中( )
| A. | NH4+、Na+、SO42-一定存在,CO32--定不存在 | |
| B. | NH4+、SO42--定存在,CO32-、Na+-定不存在 | |
| C. | c(Cl-)至少为0.2 mol/L | |
| D. | c(Fe3+)一定为0.2 mol/L |
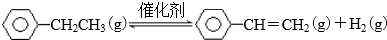
(1)一定温度下,将amol乙苯加入体积为VL的密闭容器中,发生上述反应,反应时间与容器内气体总压强的数据如下表.
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| 总压强/1000kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
②列式计算此温度下该反应的平衡常数K$\frac{4a}{15V}$
(2)根据化学反应原理,分析减小压强对该反应的影响该反应分子数增加,减小压强使平衡右移,乙苯转化率增大,苯乙烯产率增加,减小压强使乙苯浓度减小,反应速率减小
(3)实际生产的反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比对乙苯转化率的影响可用图表示.[M=n(H2O)/n(乙苯]

①比较图中A、B两点对应平衡常数大小:KA<KB
②图中投料比(M1、M2、M3)的大小顺序为M1>M2>M3
③随着反应的进行,催化剂上的少量积炭使其活性减弱,水蒸气有助于恢复催化剂的活性,原因是C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2(用化学方程式表示)
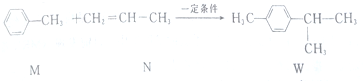 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | M的所有原子可能在同一平面上 | |
| B. | N的二氯代物有5种同分异构体(不考虑立体异构) | |
| C. | W的分子式为C10H14 | |
| D. | M、N和W均能发生氧化反应和加成反应 |
| A. | 每个53131Cs含有78个中子 | B. | CsOH的碱性比KOH的强 | ||
| C. | HI的还原性比HF的强 | D. | KIO3是碘的最高价含氧酸的盐 |
 .
.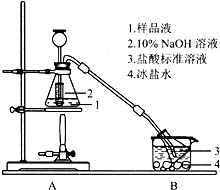 Cux(NH3)y(SO4)z•nH2O是深蓝色晶体,可溶于水,不溶于乙醇、乙醚等有机溶剂,常用作杀虫剂、媒染剂等.某小组利用废铜屑、硫酸、氨水等原料制备该晶体并测定其组成.
Cux(NH3)y(SO4)z•nH2O是深蓝色晶体,可溶于水,不溶于乙醇、乙醚等有机溶剂,常用作杀虫剂、媒染剂等.某小组利用废铜屑、硫酸、氨水等原料制备该晶体并测定其组成.