题目内容
5.已知反应:①2C( s )+O2( g)═2CO( g )△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O( l )△H=-57.3kJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀醋酸与稀NaOH溶液反应生成1mol H2O时对应的反应热为-57.3 kJ/mol | |
| D. | 稀盐酸与稀NaOH溶液反应生成1mol H2O时对应的反应热为-57.3 kJ/mol |
分析 A.CO燃烧生成二氧化碳继续放出热量;
B.反应热分吸收热量,放出热量;
C.醋酸是弱电解质,电离过程是吸热;
D.根据中和热表述方法分析.
解答 解:A.使用燃烧热时要注意两个关键点:①反应物用量:可燃物为1mol;②产物要求:充分燃烧成稳定氧化物[H→H2O(l)、C→CO2 (g)、S→SO2 (g)],由反应①可知,1mol碳燃烧生成CO放出的热量为110.5 kJ,CO燃烧生成二氧化碳继续放出热量,故1mol碳完全燃烧放出的热量大于110.5 kJ,所以碳的燃烧热大于110.5 kJ/mol,故A错误;
B.①的反应热为-221kJ/mol,故B错误;
C.醋酸的电离过程是吸热的,稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3kJ,则反应热大于-57.3 kJ/mol,故C错误;
D.稀盐酸与稀NaOH溶液反应生成1mol H2O时放出的热量为57.3kJ,则反应热为-57.3 kJ/mol,故D正确;
故选D.
点评 本题主要考查学生对于反应热、中和热的理解及有关计算等,题目难度不大,注意中和热表述方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
15.化学是以实验为基础的科学,关于下列各实验装置的叙述中,正确的是:( )
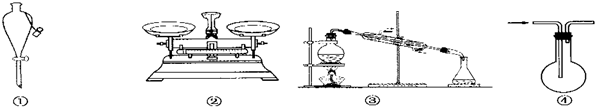

| A. | 仪器①可用于乙醇与水分离提纯 | |
| B. | 仪器②可用于称取5.85 g氯化钠固体 | |
| C. | 装置③的烧瓶中应加沸石,以防暴沸 | |
| D. | 装置④从箭头方向进气,用排空气法可收集H2 |
20.实验室配制浓度为2.0mol•L-1 NaOH溶液100mL,下面有关操作及说法正确的是( )
| A. | 配制操作为:称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| B. | 称量 NaOH固体时,应在托盘天平两盘上各放一张大小相同的纸片 | |
| C. | 若所用NaOH固体中有少量Na2O杂质,则造成所配溶液浓度偏高 | |
| D. | 若用10 mol•L-1NaOH溶液来配制,用量筒量取20 mL NaOH浓溶液倒入烧杯后,应该用同一量筒取一定量蒸馏水倒入烧杯中 |
10.关于下列的能量变化,下列说法正确的是( )
| A. | 燃烧是将化学能只转化为热能 | |
| B. | 浓硫酸溶于水发热,所以该反应为放热反应 | |
| C. | 反应物的总能量高于生成物的总能量是放热反应 | |
| D. | 吸热反应是断裂化学键吸收的总能量小于形成化学键放出的总能量 |
17.下列实验操作能达到实验目的是( )
| A. | 除去AlCl3溶液中的FeCl3杂质的方法:先加入足量浓氨水,过滤,再加入过量盐酸,得到纯净AlCl3溶液 | |
| B. | 可以用金属钠和MgCl2溶液反应置换金属Mg;可以通过化合反应制备Fe(OH)3 | |
| C. | 对某溶液进行焰色反应,火焰呈黄色,则证明该溶液中含有钠盐,可能有钾盐 | |
| D. | 配制氯化铁溶液时,将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
10.下列有机物的命名肯定错误的是( )
| A. | 4-甲基-2-戊烯 | B. | 2,2-二甲基丙烷 | ||
| C. | 2,3,3-三甲基-2-戊烯 | D. | 4-乙基-2-庚烯 |
11.相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/moL.实验测得起始、平衡时得有关数据如表:
下列叙述错误的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等 | |
| B. | 平衡时,两个容器中NH3的体积分数均为25% | |
| C. | 容器②中达平衡时放出的热量Q=23.15 kJ | |
| D. | 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ |
 .
.