题目内容
1.下列离子方程式正确的是( )| A. | HCO3-+H2O?H2CO3+OH- | B. | Al3++3H2O?Al(OH)3+3H+ | ||
| C. | 2Al3++3CO32-?Al2(CO3)3 | D. | Br-+H2O?HBr+OH- |
分析 A.碳酸氢根离子发生水解生成碳酸和氢氧根离子;
B.铝离子水解生成氢氧化铝和氢离子;
C.铝离子与碳酸根离子发生双水解反应生成氢氧化铝沉淀、二氧化碳气体;
D.HBr为强电解质,溴离子不发生水解反应.
解答 解:A.碳酸氢根离子水解的离子方程式为:HCO3-+H2O?H2CO3+OH-,故A正确;
B.铝离子水解的离子方程式为:Al3++3H2O?Al(OH)3+3H+,故B正确;
C.铝离子与碳酸根离子发生双水解反应,正确的离子方程式为:2Al3++3CO32-+3H2O?2Al(OH)3↓+3CO2↑,故C错误;
D.HBr为强电解质,Br-不发生水解,故D错误;
故选AB.
点评 本题考查了电离方程式的书写方法,题目难度不大,明确盐的水解原理为解答关键,注意掌握电离方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
11.通过化学反应不能实现的是( )
| A. | 生成一种新离子 | B. | 生成一种新分子 | C. | 生成一种新核素 | D. | 生成一种新单质 |
9.下列叙述错误的是( )
| A. | 带相反电荷离子之间的静电作用称为离子键 | |
| B. | 金属元素与非金属元素化合时,不一定形成离子键 | |
| C. | 某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键 | |
| D. | 非金属元素形成的化合物中不可能含有离子键 |
6.下列物质中,不能用金属和氯气反应制得的是( )
| A. | CuCl2 | B. | AlCl3 | C. | NaCl | D. | FeCl2 |
13.我国科学家成功地研制出长期依赖进口、价格昂贵的物质${\;}_8^{18}{O_2}$,下列说法正确的是( )
| A. | 它与${\;}_8^{16}{O_2}$的物理性质完全相同 | |
| B. | 它是O3的一种同素异形体 | |
| C. | ${\;}_8^{18}{O_2}$与${\;}_8^{16}{O_2}$互为同位素 | |
| D. | 1mol${\;}_8^{18}{O_2}$分子中含有20mol电子 |
10.能使溴水因发生化学反应而褪色,也能使酸性高锰酸钾溶液褪色的是( )
| A. | 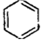 | B. | C6H14 | C. | CH3CH2OH | D. | 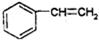 |

 .
. ,
,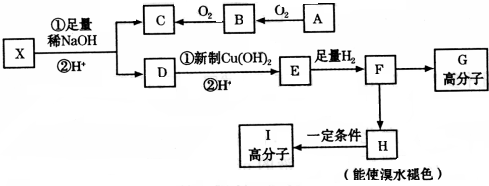
 .
. .
. .
.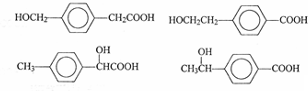 .
.