题目内容
15.对于可逆反应2AB3(g)?2A(g)+3B2(g)△H>0,下列图象不正确的是( )| A. |  | B. | 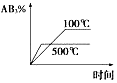 | C. | 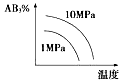 | D. | 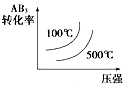 |
分析 该反应为气体体积增大、吸热的反应,升高温度平衡正向移动,增大压强平衡逆向移动,且升高温度、增大压强均加快反应速率,以此来解答.
解答 解:A.由图可知,升高温度,交叉点后正反应速率大于逆反应速率,平衡正向移动,故A正确;
B.由图可知,温度高的反应速率快,且反应物的含量低,平衡正向移动,故B正确;
C.由图可知,温度高反应物含量低、压强大反应物的含量高,则升高温度平衡正向移动,增大压强平衡逆向移动,故C正确;
D.压强越大,平衡逆向移动,反应物的转化率减小,且温度越高平衡正向移动,转化率越大,图象与平衡移动不符,故D错误;
故选D.
点评 本题考查化学平衡移动,为高考常见题型和高频考点,把握温度、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意平衡移动原理与图象的结合,题目难度不大.

练习册系列答案
相关题目
3.在下列各溶液中,一定能大量共存的离子组是( )
| A. | 常温下水电离的c(H+)为1×10-12mol/L的溶液中:Fe2+、Na+、SO42-、NO3- | |
| B. | 滴加石蕊后呈蓝色的溶液中:K+、AlO2-、Cl-、HCO3- | |
| C. | 含有大量HCO3-的澄清透明溶液中:K+、Al3+、SO42-、Na+ | |
| D. | 常温下c(OH-)/c(H+)=1014的溶液中:K+、Ba2+、Cl-、Br- |
6.下列说法正确的是( )
| A. | 甲烷分子的比例模型为  ,其二氯取代物有2种结构 ,其二氯取代物有2种结构 | |
| B. | 苯和乙烯都能使溴水褪色,其褪色原理相同 | |
| C. | 相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同 | |
| D. | 在一定条件下,苯与氯气生成氯苯的反应类型是加成反应 |
10.某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于下表:
(1)①可以判断该分解反应已经达到化学平衡的是BC.
A.2v(NH3)=v(CO2)B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=1.6×10-8(mol•L-1)3.
③氨基甲酸铵分解反应的焓变△H>0,熵变△S>0(填>、<或=).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:K=1.6×10-8(mol•L-1)3.
③氨基甲酸铵分解反应的焓变△H>0,熵变△S>0(填>、<或=).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.

计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
7.下列关于物质性质或检验的叙述不正确的是( )
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中一定有Fe3+,可能有Fe2+ | |
| B. | 气体通过湿润的红色石蕊试纸,试纸变蓝,证明原气体中一定含有氨气 | |
| C. | 用铂丝蘸取白色粉末灼烧,火焰成黄色,证明原粉末中一定有Na+,可能有K+ | |
| D. | 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- |
4.下列指定反应的化学方程式或离子方程式书写正确的是( )
| A. | 乙醇和浓硫酸混合加热至140℃,CH3CH2OH$→_{140℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| B. | 1-溴丙烷与氢氧化钠的乙醇溶液供热:CH3CH2CH2Br+NaOH$→_{△}^{乙醇}$CH3CH2CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量的CO2:2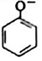 +H2O+CO2→2 +H2O+CO2→2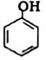 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 乙醛在碱性条件下被新制的氧化铜氧化:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+CuO↓+3H2O |
5.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 该温度下此反应的平衡常数K=1.44 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 | |
| D. | 0~2min的平均速率ν(Z)=2.0×10-3mol•L-1•min-1 |