题目内容
20.1L KNO3和Cu(NO3)2的混合溶液中c (NO3-)=4mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况下),假定电解后溶液体积仍为1L,原混合溶液中c(K+)为( )| A. | 1mol•L-1 | B. | 2mol•L-1 | C. | 3mol•L-1 | D. | 4mol•L-1 |
分析 石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),则阴极发生Cu2++2e-═Cu、2H++2e-═H2↑,阳极发生4OH--4e-═O2↑+2H2O,n(O2)=$\frac{22.4L}{22.4L/mol}$=1mol,结合电子守恒及物质的量浓度的计算来解答.
解答 解:石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),n(O2)=$\frac{22.4L}{22.4L/mol}$=1mol,
阳极发生4OH--4e-═O2↑+2H2O,
4mol 1mol
阴极发生Cu2++2e-═Cu、2H++2e-═H2↑,
1mol 2mol 1mol 2mol 1mol
c(Cu2+)=$\frac{1mol}{1L}$=1mol/L,
由电荷守恒可知,原混合溶液中c(K+)为4mol/L-1mol/L×2=2mol/L,
故选B.
点评 本题考查电解原理,明确发生的电极反应及电子守恒是解答本题的关键,题目难度中等,选项D为学生解答的难点,注意氢氧根离子与氢离子的关系即可解答.

练习册系列答案
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案
相关题目
11.常温下,下列各组离子在指定的条件下一定能大量共存的是( )
| A. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| B. | 在pH=2的溶液中:NH4+、K+、ClO-、Cl- | |
| C. | 在c(H+)/c(OH-)=10-12的溶液中:K+、Na+、C1O-、NO3- | |
| D. | 水电离c(H+)=10-12的溶液中:Mg2+、Cu2+、SO42+、K+ |
9.关于单质硫的叙述:①通常情况下为黄色粉末 ②不溶于水,易溶于酒精和CS2 ③氧化性比氯弱④只能被还原不能被氧化⑤医药上用来做硫磺软膏,治疗某些皮质病,其中正确的是( )
| A. | ①②③⑤ | B. | ②③⑤ | C. | ③④⑤ | D. | ①③⑤ |
10.下列气体组(括号内为混有的少量杂质),最适宜用CuSO4溶液进行提纯的是( )
| A. | HCl(H2S) | B. | O2(N2) | C. | CO(H2S) | D. | H2S(HCl) |
 .
. .
.
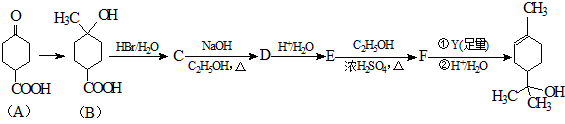
 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
.