题目内容
 氨的催化氧化是工业制硝酸的重要反应,500°C,其反应方程式为:
氨的催化氧化是工业制硝酸的重要反应,500°C,其反应方程式为:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+Q,完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是( )
a.减压 b.增加NH3的浓度 c.升温 d.将水液化移走.
(2)在500℃时,在2L密闭容器中加入10mol NH3、10mol O2,上述可逆反应达到平衡,过程如图所示,在a时刻改变反应条件,重新达到平衡,该改变的条件可能是
(3)工业上以氨和空气为原料生产硝酸,请画出硝酸工业的物质流程图.
(4)氨中氮元素原子最外层电子排布的轨道表达式是
(5)已知NH3与N2H4都是氮的氢化物,N2H4的电子式是
考点:化学反应速率的影响因素,元素周期律的作用,化学平衡的影响因素
专题:
分析:(1)影响反应速率的因素有温度、浓度、压强、催化剂以及接触面积等等;
(2)该反应为正反应气体体积增大的放热反应,a时刻后平衡逆向移动,且正逆反应速率都增大,说明改变的条件是加压或升温;b时刻到c时刻,平衡正向移动;c时刻后加压平衡正向移动,说明反应物气体物质的量高于生成物;c时刻到d时刻,加压正逆反应速率都增大且正反应速率大于逆反应速率;
(3)工业上以氨和空气为原料生产硝酸,首先是氨的催化氧化生成NO,NO再被空气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和NO,NO循环使用,据此画出硝酸工业的物质流程图;
(4)N原子最外层5个电子,分别排布在2s和2p上;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小;元素的非金属性越强,其对应氢化物越稳定;
(5)N原子最外层5个电子,有3个电子分别与N原子和2个H原子形成共价键;据原子守恒和得失电子守恒书写化学方程式.
(2)该反应为正反应气体体积增大的放热反应,a时刻后平衡逆向移动,且正逆反应速率都增大,说明改变的条件是加压或升温;b时刻到c时刻,平衡正向移动;c时刻后加压平衡正向移动,说明反应物气体物质的量高于生成物;c时刻到d时刻,加压正逆反应速率都增大且正反应速率大于逆反应速率;
(3)工业上以氨和空气为原料生产硝酸,首先是氨的催化氧化生成NO,NO再被空气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和NO,NO循环使用,据此画出硝酸工业的物质流程图;
(4)N原子最外层5个电子,分别排布在2s和2p上;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小;元素的非金属性越强,其对应氢化物越稳定;
(5)N原子最外层5个电子,有3个电子分别与N原子和2个H原子形成共价键;据原子守恒和得失电子守恒书写化学方程式.
解答:
解:(1)a.减压反应速率减慢,故错误;
b.增加NH3的浓度反应速率加快,故正确;
c.升温反应速率加快,故正确;
d.将水液化移走,降低了浓度,反应速率减慢,故错误;
故答案为:bc;
(2)该反应为正反应气体体积增大的放热反应,a时刻后平衡逆向移动,且正逆反应速率都增大,说明改变的条件是加压或升温;b时刻到c时刻,平衡正向移动,反应物转化率增大;c时刻后加压平衡正向移动,说明反应物气体物质的量高于生成物,可能是水加压被氧化;c时刻到d时刻,加压正逆反应速率都增大且正反应速率大于逆反应速率,据此画图,故答案为:升温或加压;<;可能加压后水被液化
 ;
;
(3)工业上以氨和空气为原料生产硝酸,首先是氨的催化氧化生成NO,NO再被空气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和NO,NO循环使用,据此画出硝酸工业的物质流程图为: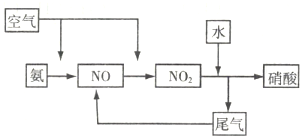 ,故答案为:
,故答案为: ;
;
(4)N原子最外层5个电子,分别排布在2s和2p上,最外层电子排布为: ;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小,电子层数越多,原子半径越大,相同电子层时,质子数越多,原子半径越小,Na>Mg>Al>O>F;元素的非金属性越强,其对应氢化物越稳定,N、O、F非金属性依次增强,所以其氢化物稳定性HF>H2O>NH3
;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小,电子层数越多,原子半径越大,相同电子层时,质子数越多,原子半径越小,Na>Mg>Al>O>F;元素的非金属性越强,其对应氢化物越稳定,N、O、F非金属性依次增强,所以其氢化物稳定性HF>H2O>NH3
故答案为: ; Na>Mg>Al>O>F;HF>H2O>NH3;
; Na>Mg>Al>O>F;HF>H2O>NH3;
(5)N原子最外层5个电子,有3个电子分别与N原子和2个H原子形成共价键,电子式为 ;氨被双氧水氧化为游离态氮,每mol氨失3mol电子,H2O2得电子生成H2O,每mol得2mol电子,所以氨分子和过氧化氢分子化学计量数之比为2:3,再据原子守恒书写化学方程式为:2NH3+3H2O2=N2+6H2O,
;氨被双氧水氧化为游离态氮,每mol氨失3mol电子,H2O2得电子生成H2O,每mol得2mol电子,所以氨分子和过氧化氢分子化学计量数之比为2:3,再据原子守恒书写化学方程式为:2NH3+3H2O2=N2+6H2O,
故答案为: ;2NH3+3H2O2=N2+6H2O.
;2NH3+3H2O2=N2+6H2O.
b.增加NH3的浓度反应速率加快,故正确;
c.升温反应速率加快,故正确;
d.将水液化移走,降低了浓度,反应速率减慢,故错误;
故答案为:bc;
(2)该反应为正反应气体体积增大的放热反应,a时刻后平衡逆向移动,且正逆反应速率都增大,说明改变的条件是加压或升温;b时刻到c时刻,平衡正向移动,反应物转化率增大;c时刻后加压平衡正向移动,说明反应物气体物质的量高于生成物,可能是水加压被氧化;c时刻到d时刻,加压正逆反应速率都增大且正反应速率大于逆反应速率,据此画图,故答案为:升温或加压;<;可能加压后水被液化
 ;
;(3)工业上以氨和空气为原料生产硝酸,首先是氨的催化氧化生成NO,NO再被空气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和NO,NO循环使用,据此画出硝酸工业的物质流程图为:
 ,故答案为:
,故答案为: ;
;(4)N原子最外层5个电子,分别排布在2s和2p上,最外层电子排布为:
 ;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小,电子层数越多,原子半径越大,相同电子层时,质子数越多,原子半径越小,Na>Mg>Al>O>F;元素的非金属性越强,其对应氢化物越稳定,N、O、F非金属性依次增强,所以其氢化物稳定性HF>H2O>NH3
;N 3-离子核外电子数为10,能够形成10电子离子的原子有 Na、Mg、Al、O、F,据已知的电子层数和质子数判断原子半径大小,电子层数越多,原子半径越大,相同电子层时,质子数越多,原子半径越小,Na>Mg>Al>O>F;元素的非金属性越强,其对应氢化物越稳定,N、O、F非金属性依次增强,所以其氢化物稳定性HF>H2O>NH3故答案为:
 ; Na>Mg>Al>O>F;HF>H2O>NH3;
; Na>Mg>Al>O>F;HF>H2O>NH3;(5)N原子最外层5个电子,有3个电子分别与N原子和2个H原子形成共价键,电子式为
 ;氨被双氧水氧化为游离态氮,每mol氨失3mol电子,H2O2得电子生成H2O,每mol得2mol电子,所以氨分子和过氧化氢分子化学计量数之比为2:3,再据原子守恒书写化学方程式为:2NH3+3H2O2=N2+6H2O,
;氨被双氧水氧化为游离态氮,每mol氨失3mol电子,H2O2得电子生成H2O,每mol得2mol电子,所以氨分子和过氧化氢分子化学计量数之比为2:3,再据原子守恒书写化学方程式为:2NH3+3H2O2=N2+6H2O,故答案为:
 ;2NH3+3H2O2=N2+6H2O.
;2NH3+3H2O2=N2+6H2O.
点评:本题考查了影响化学反应速率的因素和影响平衡移动的因素以及高于制硝酸、核外电子排布、原子半径大小比较、非金属性强弱比较、氧化还原反应方程式书写,题目跨度大,难度中等.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
下列常用实验仪器中,用来配制一定物质的量浓度的是( )
| A、分液漏斗 | B、普通漏斗 |
| C、蒸馏烧瓶 | D、容量瓶 |
常温下,浓度均为1.0mol?L-1的NH3?H2O和NH4Cl混合溶液10mL,测得其pH为9.3.下列有关叙述正确的是( )
| A、加入适量的NaCl,可使c(NH4+)=c(Cl-) | ||||
| B、滴加几滴浓氨水,c(NH4+)减小 | ||||
C、滴加几滴浓盐酸,
| ||||
| D、1.0 mol?L-1的NH4Cl溶液中c(NH4+)比该混合溶液大 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、水电离出的c(OH-)=0.001mol/L的溶液:H+、Fe 2+、Cl-、SO4 2- |
| B、c(H+)=0.001mol/L的溶液:NH4+、Ba 2+、A1O2-、Cl- |
| C、pH=12的溶液:K +、Fe 2+、ClO-、Br- |
| D、与铝反应产生大量氢气的溶液:Na+、NH4+、Cl-、NO3- |
下列实验操作中,错误的是( )
①在托盘天平上用滤纸称取4.0gNaOH;
②用10mL 量筒量取5.25mL盐酸;
③用蒸发皿加热KNO3溶液制取KNO3晶体;
④用100mL容量瓶配制60mL 1mol?L-1 H2SO4溶液;
⑤用带玻璃塞的棕色试剂瓶存放AgNO3溶液;
⑥用50mL蒸馏烧瓶加热40mL乙酸乙酯和乙酸的混合液,分离出乙酸乙酯.
①在托盘天平上用滤纸称取4.0gNaOH;
②用10mL 量筒量取5.25mL盐酸;
③用蒸发皿加热KNO3溶液制取KNO3晶体;
④用100mL容量瓶配制60mL 1mol?L-1 H2SO4溶液;
⑤用带玻璃塞的棕色试剂瓶存放AgNO3溶液;
⑥用50mL蒸馏烧瓶加热40mL乙酸乙酯和乙酸的混合液,分离出乙酸乙酯.
| A、②④⑥ | B、①②③⑥ |
| C、①②⑥ | D、③④⑤ |
下列分子式表示的有机物中,含单官能团的同分异构体数目最多的是( )
| A、C4H10O |
| B、C4H10 |
| C、C3H6O |
| D、C4H7Cl |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、58 g乙烯和乙烷的混合气体中碳原子数目一定为4NA |
| B、用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA |
| C、已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA |
| D、142g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA |
下列叙述正确的是( )
| A、实验室制取蒸馏水的装置中冷水从冷凝管的上口进,下口出 |
| B、任何可燃性气体点燃前都必须检验纯度 |
| C、NaCl溶液蒸发结晶时,蒸发皿中刚有晶体析出即停止加热 |
| D、氢氧化铁胶体中滴加少量稀硫酸,因发生化学反应而沉淀 |
