题目内容
(6分)(1)已知0.1mol/L的NaHSO4溶液中H+ 的物质的量浓度为0.1mol/L,请回答下列问题:
①写出NaHSO4在水溶液中电离的方程式:___________________________________。
②若将NaHSO4与Ba(OH)2在溶液中按物质的量比为2:1混合,反应的离子方程式是:___________________________________________________________。
若将NaHSO4与Ba(OH)2在溶液中按物质的量比为1:1混合,反应的离子方程式是:___________________________________________________________。
(6分)NaHSO4=Na++H++SO42- (2分);2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O (2分) ;
H++SO42-+OH-+ Ba2+=BaSO4↓+H2O (2分) ;
【解析】
试题分析:①由0.1mol/L的NaHSO4溶液中H+ 的物质的量浓度为0.1mol/L,知NaHSO4是强酸的酸式盐,酸式酸根完全电离,即NaHSO4=Na++H++SO42- 。
②若将NaHSO4与Ba(OH)2在溶液中按物质的量比为2:1混合,H+与OH-完全中和,Ba2+与SO42-不完全反应,SO42-有乘余。若将NaHSO4与Ba(OH)2在溶液中按物质的量比为1:1混合,Ba2+与SO42-完全反应,H+与OH-不完全反应,OH-有乘余。离子方程式分别为2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O ;H++SO42-+OH-+ Ba2+=BaSO4↓+H2O
考点:NaHSO4的性质及离子方程式

 阅读快车系列答案
阅读快车系列答案
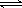 2SO3(g),下列判断不正确的是
2SO3(g),下列判断不正确的是 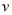 正(O2)=
正(O2)=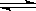 C (g)+D(g) 已达到平衡状态的是
C (g)+D(g) 已达到平衡状态的是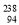 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于 Pu的说法正确的是
Pu的说法正确的是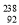 U互为同位素
U互为同位素  Pu为同一种核素
Pu为同一种核素