题目内容
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )| A、元素Y和元素Z的最高正化合价相同 |
| B、单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C、气态氢化物稳定性:X<Y<Z |
| D、元素W的最高价氧化物对应的水化物是强酸 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,Y原子的最外层电子数是次外层电子数的3倍,次外层电子数为2,最外层电子数为6,则Y为O元素;由图中的位置可知,X为N,Z为S,W为Cl,然后利用元素周期律及物质的性质来解答.
解答:
解:X、Y、Z、W均为短周期元素,Y原子的最外层电子数是次外层电子数的3倍,次外层电子数为2,最外层电子数为6,则Y为O元素;由图中的位置可知,X为N,Z为S,W为Cl,
A.氧元素一般没有正化合价,故A错误;
B.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->O2-,故B错误;
C.非金属性O>N>S,则氢化物稳定性H2O>NH3>H2S,故C错误;
D.W为Cl元素,最高价含氧酸HClO4是最强的含氧酸,故D正确;
故选D.
A.氧元素一般没有正化合价,故A错误;
B.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->O2-,故B错误;
C.非金属性O>N>S,则氢化物稳定性H2O>NH3>H2S,故C错误;
D.W为Cl元素,最高价含氧酸HClO4是最强的含氧酸,故D正确;
故选D.
点评:本题考查位置结构性质的相互关系应用,题目难度不大,正确推断元素的种类为解答该题的关键,注意把握元素周期律的递变规律,C为易错点,学生容易忽略过氧化氢,注意O、F元素一般没有正化合价.

练习册系列答案
相关题目
下列除去括号内杂质的试剂及方法有错误的是( )
| A、FeCl2(FeCl3)→足量氯气 |
| B、Fe(Al)→NaOH溶液,过滤,洗涤 |
| C、MgCl2(AlCl3)→足量NaOH溶液,过滤,盐酸 |
| D、Fe2O3(SiO2)→NaOH溶液,过滤 |
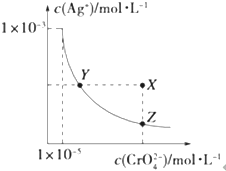 在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法不正确的是( )
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法不正确的是( )| A、t℃时,Ag2CrO4的Ksp为1×10-11 |
| B、饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点 |
| C、t℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| D、t℃时,将0.01mol?L-1AgNO3溶液滴入20mL0.01mol?L-1KCl和0.01mol?L-1K2CrO4的混合溶液中,Cl-先沉淀 |
下列说法正确的是( )
| A、分别中和等体积、等pH的盐酸和醋酸,消耗的NaOH物质的量相同 |
| B、在0.1mol.L-1NaHSO3溶液中有c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
| C、将AgCl和AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,只有AgBr沉淀的生成 |
| D、测定某酸的钠盐溶液常温下的pH,若pH>7,则说明该酸是弱酸 |
对于CH3COOH、HCl、H2SO4三种溶液,下列判断正确的是( )
| A、pH相同的三种溶液,物质的量浓度最小的是HCl |
| B、物质的量浓度相同的三种溶液,pH最小的是H2SO4 |
| C、含溶质的物质的量相同的三种溶液与过量镁粉反应,CH3COOH产生的H2最多 |
| D、相同pH、相同体积的三种溶液用NaOH溶液完全中和时,消耗NaOH溶液一样多 |
氢气是一种清洁的可再生能源.上海最新研发的“超越”3号氢燃料电池轿车,每行驶100km仅耗氢气1kg左右,同时消耗氧气约为( )
| A、250mol | B、500mol |
| C、8kg | D、16kg |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4LCCl4含有C-Cl键的数目为4NA | ||||
| B、取50mL 14.0mol/L浓硝酸与足量铜片反应,生成气体分子的数目为0.35 NA | ||||
C、反应NH4N3
| ||||
| D、电解精炼铜时,若转移的电子数为NA个,则阳极质量减小32g |