题目内容
下列实验事实不能用平衡移动原理解释的是( )
A、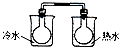 NO2球浸在冷水和热水中 | ||||||||
B、
| ||||||||
C、 | ||||||||
D、
|
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答:
解:A、2NO2?N2O4,△H<0,升高温度,平衡逆向移动,颜色加深,降低温度,平衡正向移动,颜色变浅,能用平衡移动原理解释,故A错误;
B、水的电离平衡是吸热的过程,升高温度,平衡正向移动,水的离子积常数变大,能用平衡移动原理解释,故B错误;
C、催化剂不会引起平衡的移动,只能同等程度的改变正逆反应速率,故C正确;
D、氨水的电离过程是吸热的过程,升高温度,平衡正向移动,碱性增强,pH变大,能用平衡移动原理解释,故D错误;
故选C.
B、水的电离平衡是吸热的过程,升高温度,平衡正向移动,水的离子积常数变大,能用平衡移动原理解释,故B错误;
C、催化剂不会引起平衡的移动,只能同等程度的改变正逆反应速率,故C正确;
D、氨水的电离过程是吸热的过程,升高温度,平衡正向移动,碱性增强,pH变大,能用平衡移动原理解释,故D错误;
故选C.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、1mol钠与O2反应生成Na2O 或Na2O2,转移的电子数目均为2NA |
| B、1molO2和足量的Mg或Al完全反应,电子转移数目之比为2:3 |
| C、Na、Mg、Al各1mol和足量的O2反应,电子转移数目之比为1:2:3 |
| D、Cu、Mg各1mol在O2中充分燃烧,电子转移数目之比为3:2 |
确定乙酸是弱酸的依据是( )
| A、乙酸可以和乙醇发生酯化反应 |
| B、乙酸钠的水溶液显碱性 |
| C、乙酸能使石蕊试液变红 |
| D、Na2CO3中加入乙酸产生CO2 |
下述反应在5L密闭容器中进行4NH3(g)+5O2(g)=4NO(g)+6H2O(g)半分钟后,NO物质的量增加了0.3mol,则此反应的平均速率v(x)表示反应物的消耗速率或生成物的生成速率)为( )
| A、v(NO)=0.001 mol/(L?s) |
| B、v(H2O)=0.001 mol/(L?s) |
| C、v(NH3)=0.002 mol/(L?s) |
| D、v(O2)=0.015mol/(L?s) |
下列电解质的电离方程式书写正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、KClO3═K++Cl-+3O2- |
| C、NaHSO4═Na++H++SO42- |
| D、NH3?H2O═NH4++OH- |
Na2O2中氧的化合价是( )
| A、-1 | B、-2 | C、+1 | D、+2 |
下列高聚物必须由两种单体加聚而成的是( )
A、 |
B、 |
C、 |
D、 |
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A、原子半径:W>Z>Y>X |
| B、含Y元素的盐溶液一定显酸性 |
| C、最简单气态氢化物的热稳定性:Z>W |
| D、X与氢元素组成的化合物XH5与水反应可产生两种气体 |