题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、7.8gNa2O2中阴、阳离子总数为0.4NA |
| B、4.4gCO2和C3H8的混合气体中含有的分子总数为0.1NA |
| C、0.1mol苯乙烯中含碳碳双键总数为0.4NA |
| D、标准状况下,1.12L乙酸中含有氢原子总数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.7.8g Na2O2固体物质的量为0.1mol;
B.CO2和C3H8的摩尔质量都是44g/mol;
C.一个苯乙烯分子中只含有1个碳碳双键;
D.乙酸是液体.
B.CO2和C3H8的摩尔质量都是44g/mol;
C.一个苯乙烯分子中只含有1个碳碳双键;
D.乙酸是液体.
解答:
解:A.过氧化钠是钠离子和过氧根离子构成,0.1mol过氧化钠含离子数0.3mol离子,故A错误;
B.CO2和C3H8的摩尔质量都是44g/mol,4.4gCO2和C3H8的混合气体的物质的量为0.1mol,分子总数为0.1NA,故B正确;
C.一个苯乙烯分子中只含有1个碳碳双键,0.1mol苯乙烯中含碳碳双键数为0.1NA,故C错误;
D.乙酸是液体,1.12L乙酸的物质的量不是0.05mol,故D错误.
故选B.
B.CO2和C3H8的摩尔质量都是44g/mol,4.4gCO2和C3H8的混合气体的物质的量为0.1mol,分子总数为0.1NA,故B正确;
C.一个苯乙烯分子中只含有1个碳碳双键,0.1mol苯乙烯中含碳碳双键数为0.1NA,故C错误;
D.乙酸是液体,1.12L乙酸的物质的量不是0.05mol,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数有关计算,难度不大,注意气体摩尔体积的使用范围和条件,C选项是难点.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
下列有关说法体现了化学与生产、生活、社会的密切关系. 其中不正确的是( )
| A、绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 |
| B、为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、停车场安装催化光反应设施,可使汽车尾气中的CO和NOX反应生成无毒气体 |
| D、氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料 |
为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念:AG=1g
,则下列叙述不正确的是( )
| c(H+) |
| c(OH-) |
| A、中性溶液的AG=0 |
| B、碱性溶液的AG>0 |
| C、AG越小碱性越强,酸性越弱 |
| D、常温下0.1mol?L-1氢氧化钠溶液的AG=-12 |
下列叙述正确的是( )
| A、SiO2和A12O3都既能与酸反应,又能与碱反应 |
| B、硫化钠溶于水中发生反应的离子方程式为S2-+2H2O?H2S+2OH- |
| C、3.2 g Cu与5.5 mL l8.4 mol?L -1的浓H2SO4充分反应,转移的电子数为6.02×1022 |
| D、由水电离的c(H+)=1×10 -13mol?L -1的溶液中Cl-、HCO3-、NO3-、NH4+能大量共存 |
居室装修用石材的放射性常用
Ra作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖.下列叙述中正确的是( )
88 22 |
A、一个
| ||
| B、Ra元素位于元素周期表中第六周期ⅡA族 | ||
| C、RaCl2难溶于水 | ||
| D、Ra(OH)2是一种两性氢氧化物 |
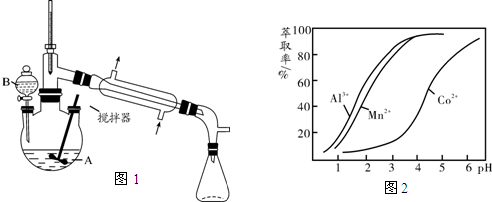
 磷化硼是一种高折射率红棕色晶体,可通过单质B与Zn3P2(或PH3)反应,也可热解PCl3?BCl3制得.
磷化硼是一种高折射率红棕色晶体,可通过单质B与Zn3P2(或PH3)反应,也可热解PCl3?BCl3制得. 其反应的装置示意图如图1(夹持装置、加热装置略去):
其反应的装置示意图如图1(夹持装置、加热装置略去):