题目内容
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁).现用如图所示的装置模拟上述过程进行试验. 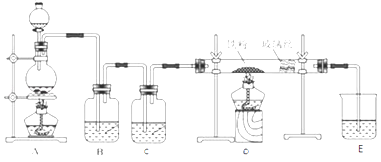
回答下列问题:
(1)盛装浓盐酸的仪器名称为 , 进行实验时,应先点燃(选填A或C)处酒精灯,装置B中加入的试剂是 , 装置C中加入的试剂 , 检验FeCl3的常用试剂为 .
(2)制取无水氯化铁的实验中,A中反应的离子方程式为 .
(3)若无B装置,反应尾气成分为 , 用E装置吸收尾气可能存在的问题、
【答案】
(1)分液漏斗; A;饱和氯化钠溶液;浓硫酸; KSCN
(2)MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(3)Cl2、H2、HCl;倒吸; H2无法吸收
【解析】解:(1)盛装浓盐酸的仪器名称为分液漏斗,进行实验时,应先点燃A处酒精灯,防止Fe与氧气反应;装置B中加入的试剂是饱和氯化钠溶液,用于除去HCl,装置C中加入的试剂浓硫酸,可干燥氯气,检验FeCl3的常用试剂为KSCN,溶液为血红色,
所以答案是:分液漏斗;A;饱和氯化钠溶液;浓硫酸;KSCN;(2)制取无水氯化铁的实验中,A中反应的离子方程式为MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O,
Mn2++Cl2↑+2H2O,
所以答案是:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;(3)若无B装置,Fe与HCl反应生成氢气,D处发生2Fe+3Cl2
Mn2++Cl2↑+2H2O;(3)若无B装置,Fe与HCl反应生成氢气,D处发生2Fe+3Cl2 ![]() 2FeCl3,反应尾气成分为Cl2、H2、HCl,用E装置吸收尾气可能存在的问题为倒吸、H2无法吸收,
2FeCl3,反应尾气成分为Cl2、H2、HCl,用E装置吸收尾气可能存在的问题为倒吸、H2无法吸收,
所以答案是:Cl2、H2、HCl;倒吸;H2无法吸收.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目



