题目内容
(1)1.5mol H2SO4含有 molH,含 molO即 个O.
(2)3.01×1023个Fe的物质的量 mol;64g氧气的物质的量 mol.
(2)3.01×1023个Fe的物质的量
考点:物质的量的相关计算
专题:计算题
分析:(1)硫酸分子中所含某原子的物质的量为硫酸的物质的量×一个硫酸分子含有的该原子数,个数通过N=n?NA计算;
(2)通过N=n?NA计算物质的量,通过n=
计算物质的量.
(2)通过N=n?NA计算物质的量,通过n=
| m |
| M |
解答:
解:(1)因1个H2SO4分子中含有2个H原子、4个O原子,则1.5molH2SO4中含3molH原子、6 molO原子,氧原子的个数为6mol×NA mol-1=6NA,
故答案为:3;6;6NA;
(2)n(Fe)=
=0.5mol,n(O2)=
=2mol,
故答案为:0.5;2.
故答案为:3;6;6NA;
(2)n(Fe)=
| 3.01×1023 |
| 6.02×1023mol-1 |
| 64g |
| 32g/mol |
故答案为:0.5;2.
点评:本题考查物质的量的简单计算,明确物质的构成及微粒数与物质的量的关系即可解答,属于基础性习题.

练习册系列答案
相关题目
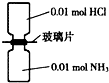 NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )
NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )| A、反应前气体的总体积为0.448L |
| B、生成物中含有0.01NA个分子 |
| C、装置中氢元素的总质量为0.04g |
| D、生成物完全溶于水后所得溶液含有0.01NA个NH4+ |
在实验室要从煤焦油中提取少量苯酚需要用到的试剂合适的是( )
| A、浓溴水、NaOH溶液 |
| B、CO2气体、NaOH溶液 |
| C、酒精 |
| D、NaOH溶液、稀HCl |
下列实验操作或装置符合实验要求的是( )
A、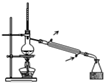 用如图装置可用于分离互不相溶的液体 |
B、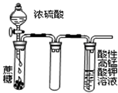 用如图装置酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、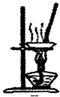 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
D、 用如图确认CO2和NaOH已发生反应 |