题目内容
16.盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂.请回答下列各问:(1)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜.下列制备方法符合“绿色化学”思想的是③(填序号).
①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu $→_{△}^{空气}$ CuO$\stackrel{HNO_{3}(稀)}{→}$Cu(NO3)2
(2)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为Cu+H2O2+2HCl=CuCl2+2H2O.
(3)围绕浓硫酸的化学性质进行了如下实验探究:①将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀.②加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体.请回答:
①黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,该反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+2SO2↑.
②写出两种可以鉴别(1)中产生的两种气体的试剂:高锰酸钾、溴水.
分析 (1)“绿色化学”是指:化学反应中没有污染性的物质生成、原子利用率高的反应;
(2)盐酸不能与金属铜反应,但可以与氧化铜反应,所以双氧水的作用是将金属铜氧化为CuO,然后氧化铜溶于盐酸;
(3)①蔗糖脱水反应生成碳,浓硫酸与碳反应生成二氧化硫、二氧化碳和水;
②二氧化硫具有还原性、二氧化碳没有还原性.
解答 解:(2)①Cu+HNO3(浓)→Cu(NO3)2,反应产生二氧化氮有毒气体,故不选;
②Cu+HNO3(稀)→Cu(NO3)2,反应生成一氧化氮有毒气体,故不选;
③Cu $→_{△}^{空气}$ CuO$\stackrel{HNO_{3}(稀)}{→}$Cu(NO3)2,反应没有有毒气体生成,硝酸全部转化为硝酸铜,原子利用率高考符合“绿色化学”思想,故选;
故答案为:③;
(2)盐酸不能与金属铜反应,但可以与氧化铜反应,所以双氧水的作用是将金属铜氧化为CuO,然后氧化铜溶于盐酸,反应的方程式为Cu+H2O2+2HCl=CuCl2+2H2O;
故答案为:Cu+H2O2+2HCl=CuCl2+2H2O;
(3)蔗糖脱水反应生成碳,浓硫酸与碳反应生成二氧化硫、二氧化碳和水,其反应的方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+2SO2↑;
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+2SO2↑;
②二氧化硫具有还原性能使高锰酸钾、溴水等褪色,二氧化碳没有还原性,不能使高锰酸钾、溴水,可以鉴别二者;
故答案为:高锰酸钾、溴水.
点评 本题考查了Cu、硝酸、浓硫酸性质及其应用,题目难度中等,明确发生反应的原理为解答关键,试题侧重考查学生灵活应用基础知识的能力.

 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案| A. | 向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| B. | 硫酸铝钾溶液中滴加氢氧化钡直到沉淀质量最大:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | |
| C. | 硫氢化钠发生电离:HS-+H2O═H3O++S2- | |
| D. | 用食醋检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+═Ca2++H2O+CO2↑ |
| A | B | C | D |
| A12O3 | Si | Na2O2 | Na2SiO3 |
| 两性氧化物 | 单质 | 碱性氧化物 | 正盐 |
| 工业用电解法冶炼铝 | 制作太阳能电池 | 用于呼吸面具作为氧气的来源 | 制备硅胶 |
| A.A | B.B | C.C | D.D |
| A. | 分子晶体 | B. | 离子晶体 | C. | 原子晶体 | D. | 以上晶体都不是 |
| A. | 硫酸铜和铝:2Al+3Cu2+═3Cu+2Al3+ | |
| B. | 氧化铜与盐酸反应:O2-+2H+═H2O | |
| C. | 碳酸钡与盐酸:CO32-+2H+═H2O+CO2↑ | |
| D. | Cu(OH)2加入H2SO4:2H++Cu(OH)2═Cu2++2H2O |
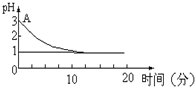 关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点:
关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点: