题目内容
为什么浓度对化学反应速率的影响,只适用于溶液或气体间的反应,而不适用于固体或液体与气体间的反应?
影响化学反应速率的因素之一就是碰撞机会,气体与固体及气体与液体间的碰撞在表面进行,它们的“浓度”是一常数。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案(1)将水蒸气通过红热的碳即可产生水煤气,其反应为C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mol-1,
①该反应在
②煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
(2)利用水煤气作为合成气,在同一个容器中,选择双催化剂,经过如下三步反应,最终合成二甲醚,此工艺称之为“一步法”合成二甲醚.
| 反应过程 | 化学方程式 | △H(kJ?mol-1) |
| 甲醇合成反应 | 2H2(g)+CO(g)=CH3OH(g) | -90.8 |
| 水煤气变换反应 | CO(g)+H2O(g)═CO2(g)+H2(g) | -41.3 |
| 甲醇脱水反应 | 2CH3OH(g)=CH3OCH3(g)+H2O(g) | -23.5 |
②该反应在一定条件下的密闭容器中达到平衡后,为同时提高化学反应速率和二甲醚的产率,可以采取的措施是
a.降低温度 b.缩小容器体积 c.加入催化剂
d.增加H2的浓度 e.分离出二甲醚
(3)控制反应条件,水煤气作为合成气也可以用来合成甲醇.在相同条件下合成二甲醚和合成甲醇的原料转化率随氢碳比的变化如图所示:
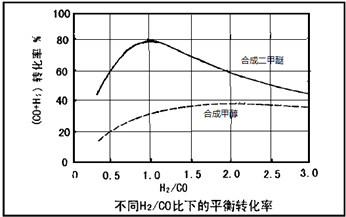
①合成二甲醚的最佳H2/CO比为
②以水煤气作为原料气,在相同条件下一步法合成二甲醚的转化率为什么明显高于合成甲醇的转化率
(14分)某课外兴趣小组的同学向Na2SiO3溶液中滴加盐酸,预计会生成H2SiO3胶体,用激光笔照射会出现“丁达尔现象”。但令人意想不到的是,试管中在出现硅酸胶体的同时也出现了大量气泡,为什么会出现这种现象呢?甲乙两同学进行了大胆的推测。
甲同学推测是生成了硅酸胶体,造成HCl在溶液中的溶解度变小,最终从溶液中逸出;
乙同学咨询了实验员得知这瓶Na2SiO3溶液已经放置很长一段时间,他推测溶液可能已经变质,故导致以上现象的出现。
(1)请设计一个最简单的实验验证甲同学的推测是否正确: ;
(2)乙同学取这瓶久置的硅酸钠溶液,用激光笔照射,发现有光柱出现,说明在这瓶硅酸钠溶液中已经有 胶体生成。推测产生的气体可能是 ,然后乙同学又做了两个实验进行验证:
I取少量该瓶溶液,向其中滴加 ,并检验产生的气体。请写出检验该气体的常用方法: ;
II取硅酸钠固体,配成饱和溶液,现配现用,滴入盐酸,观察现象;
通过以上实验,证明了乙同学观点,请写出所对应的化学反应方程式:
、 ;
该小组同学还发现按教材所述的操作方法和条件制备硅酸胶体,有时需要很长时间才能使溶胶慢慢凝聚,甚至不易形成凝胶,效果很不理想。因此,该组同学又对实验条件和操作进行探究,相关实验数据如下表:
|
|
硅酸钠溶液浓度 |
盐酸浓度 |
试剂加入顺序 |
出现凝胶时间(s) |
|
实验1 |
饱和溶液 |
1:2(盐酸和水体积比,下同) |
将Na2SiO3溶液滴加到稀盐酸中 |
21 |
|
实验2 |
稀溶液(1体积饱和溶液和3体积水混合) |
1:2 |
将稀盐酸滴加到Na2SiO3溶液中 |
38 |
|
实验3 |
饱和溶液 |
1:4 |
将Na2SiO3溶液滴加到稀盐酸中 |
10 |
|
实验4 |
稀溶液(1体积饱和溶液和3体积水混合) |
1:4 |
将稀盐酸滴加到Na2SiO3溶液中 |
50 |
该组部分同学通过实验得出结论:使用饱和Na2SiO3溶液和稀盐酸,将Na2SiO3溶液滴加到稀盐酸中效果较好。但该组另外一部分同学认为基于限定的条件,该探究实验设计组数不够,不能保证结论的准确性,要使实验具有说服力至少要做组实验。
(08枣庄三诊)氨在国民经济中占有重要的地位。现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。例如,农业上使用的氮肥如尿素、硝酸铵、磷酸铵、硫酸铵、氯化铵、氨水以及各种含氮混合肥料和复合肥料,都是以氨为原料制成的;氨氧化法制硝酸是工业上制硝酸的主要方法。
|
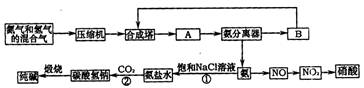
(1)下图是合成氨和利用氨制取硝酸、纯碱的简要流程示意图:
设备A的名称是 ,设备B的名称是 。
(2)硝酸厂的尾气中含有NO和NO2等污染物,籽了防止污染大气可以用纯碱溶液吸收从吸收塔中放出的尾气,发生的反应如下:Na2CO3+2NO2====NaNO2+NaNO3+CO2
但在实际生的中这种方法处理后尾气中的氮的氧化物含量仍难以降到排放标准,历此,也常利用各种燃料气中的甲烷等将氮的氧化物还原为空气主要成分而除去。写出甲烷与NO2反应的化学反应方程式: 。
(3)常压法生产出的硝酸浓度低,尾气中氮的氧化物含量高,对环境会有严重污染。可采用 法和 法进行改进。
(4)在纯碱制造过程中,过程①与过程②的顺序能否颠倒?为什么 。