题目内容
以0.10mol/L的氢氧化钠溶液滴定某一元弱酸的滴定曲线如图所示.横轴为加入氢氧化钠的体积数,纵轴为溶液的pH.下列正确的是( )


| A、此一元弱酸的电离常数(Ka)约为1.0×10-6 |
| B、此弱酸的浓度为1×10-4mol/L |
| C、此实验最好选用甲基红(变色范围在4.2~6.3)作指示剂 |
| D、此滴定反应为吸热反应 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A、依据平衡常数概念计算近似值;
B、由图象可知,当V=10mL,酸碱恰好中和;HA是弱酸,不完全电离,结合图象分析;
C、氢氧化钠和弱酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂;
D、酸碱中和反应是放热反应.
B、由图象可知,当V=10mL,酸碱恰好中和;HA是弱酸,不完全电离,结合图象分析;
C、氢氧化钠和弱酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂;
D、酸碱中和反应是放热反应.
解答:
解:A、由图象分析可知,c(H+)=1×10-4mol?L-1,但HA是弱酸,不完全电离,所以HA的浓度为大于1×10-4mol?L-1,由图象可知,当V=10mL,酸碱恰好中和,一元弱酸电离程度近似为1%,所以弱酸起始浓度为10-2mol/L,平衡常数≈
=10-6,故A正确;
B、由图象可知,当V=10mL,酸碱恰好中和,一元弱酸电离程度近似为1%,所以弱酸起始浓度为10-2mol/L,故B错误;
C、氢氧化钠和弱酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂,不能选择甲基橙,应选择酚酞指示剂,故C错误;
D、酸碱中和反应是放热反应,故D错误.
故选A.
| 10-4×10-4 |
| 10-2 |
B、由图象可知,当V=10mL,酸碱恰好中和,一元弱酸电离程度近似为1%,所以弱酸起始浓度为10-2mol/L,故B错误;
C、氢氧化钠和弱酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂,不能选择甲基橙,应选择酚酞指示剂,故C错误;
D、酸碱中和反应是放热反应,故D错误.
故选A.
点评:本题考查酸碱混合的定性判断和计算,题目难度中等,本题注意把握弱电解质的电离特点,易错点为C,注意酸碱中和滴定的实验原理.

练习册系列答案
相关题目
下列物质属于纯净物的是( )
| A、雾霾 | B、盐酸 | C、碘酒 | D、液氯 |
压强变化不会使下列化学反应的平衡发生移动的是( )
| A、H2(g)+I2(g)?2 HI(g) |
| B、3H2(g)+N2(g)?2NH3(g) |
| C、2SO2(g)+O2(g)?2SO3(g) |
| D、C(s)+CO2(g)?2CO(g) |
下列图示与对应的叙述不相符的是( )
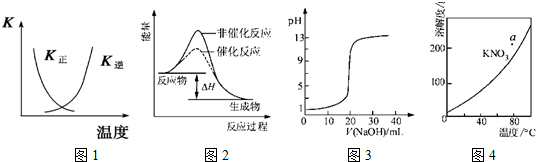

| A、图1表示该可逆反应平衡后,随温度升高,平衡会逆向移动 |
| B、图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C、图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液所得到的滴定曲线 |
| D、图4表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的过饱和溶液 |
下列说法中正确的是.
| A、1molH2SO4与1molBa(OH)2完全中和所放出的热量为中和热 |
| B、中和反应都是放热反应 |
| C、氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量高 |
| D、CO燃烧是吸热反应 |
 最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
