题目内容
18.碳及其化合物有广泛的用途.(1)反应C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是BC.
A.增加碳的用量 B.升高温度 C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1
则反应 CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ•mol-1.
(3)CO与H2一定条件下反应生成甲醇(CH3OH),可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池负极反应式为CH3OH(g)+H2O-6e-=CO2+6H+.
(4)在一定温度下,将CO(g)和H2O(g)各0.16mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②该温度下,此反应的平衡常数K=$\frac{9}{25}$;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数不变(填“增大”、“减小”或“不变”).
分析 (1)该反应是一个反应前后气体体积增大的吸热反应,升高温度、减小压强、减少生成物的量都能使平衡向正反应方向移动;
(2)利用盖斯定律构造目标热化学方程式,反应热也进行相应的运算;
(3)依据原电池原理分析,燃料电池是燃料在负极失电子发生氧化反应,正极是氧气得到电子发生还原反应,依据电解质溶液时酸性溶液书写电极反应;
(4)①正反应放热,降温时平衡正向移动;
②平衡常数表达式为K=$\frac{生成物浓度的幂次方}{反应物浓度的幂次方}$;
③反应前后气体体积不变,等比例加入反应物,平衡与原平衡等效.
解答 解:(1)A.增加碳的用量,浓度不变,平衡不移动,故错误;
B.升高温度,平衡正向移动,H2产率增大,故正确;
C.用CO吸收剂除去CO,平衡正向移动,H2产率增大,故正确;
D.加入催化剂,平衡不移动,故错误;
故选:BC;
(2)已知:①C(s)+H2O(g)?CO(g)+H2(g),△H=+131.3kJ•mol-1,
②C(s)+CO2(g)?2CO(g),△H=+172.5kJ•mol-1
根据盖斯定律,①-②得:CO(g)+H2O(g)?CO2(g)+H2(g),△H=131.3kJ•mol-1-172.5kJ•mol-1=-41.2kJ•mol-1,
故答案为:-41.2kJ•mol-1;
(3)甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,负极电极反应为:CH3OH?6e-+8OH-═CO32-+6H2O
故答案为:CH3OH(g)+H2O-6e-=CO2+6H+;
(4)①正反应放热,降温时平衡正向移动,v(正)>v(逆),故答案为:<;
②CO和H2O反应了0.06mol,则CO2和H2生成了0.06mol,平衡时各物质的浓度为:反应物CO和H2O为0.05mol/L,生成物CO2和H2为0.03mol/L,平衡常数表达式为K=$\frac{生成物浓度的幂次方}{反应物浓度的幂次方}$=$\frac{0.03mol/L×0.03mol/L}{0.05mol/L×0.05mol/L}$=$\frac{9}{25}$,故答案为:$\frac{9}{25}$;
③反应前后气体体积不变,与原平衡等比例加入反应物,平衡与原平衡等效,所以,平衡时各物质的浓度与原判断相同,故答案为:不变.
点评 本题主要考查了平衡移动、盖斯定律应用、平衡常数的计算、等效平衡,题目难度中等.

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案| A. | 常温下SO3是液体 | |
| B. | 标准状况下,1 mol SO3的体积约为22.4L | |
| C. | SO3与CaO反应生成CaSO3 | |
| D. | SO2遇空气即生成SO3 |
| A | B | C | D |
| NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾[KAl(SO4)2•12H2O]溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
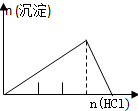 | 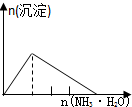 | 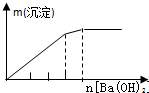 | 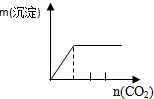 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
| A. | HNO3溶液 | B. | Ba(OH)2溶液 | C. | H2SO4溶液 | D. | HCl溶液 |
| A. | 饱和NaHCO3溶液中通入过量CO2:CO32-+CO2+H2O═HCO3- | |
| B. | 金属铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | Ca(OH)2溶液与Na2CO3溶液反应:Ca2++CO32-═CaCO3↓ | |
| D. | 氯化铝与过量氨水反应:Al3++4OH-═AlO2-+2H2O |
| A. | CaO | B. | NH4Cl | C. | H2O | D. | NaCl |
| A. | 蒸发 | B. | 萃取 | C. | 液体过滤 | D. | 升华 |
(1)制取H2和CO通常采用:C(s)+H2O(g)═CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是AD.
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成ILH2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)═C(s)+H2O(l)△H=-QkJ•mol-1,则Q<131.4
D.若C(s)+CO2(g)═2CO(g)△H1;CO(g)+H2O(g)═H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g)═CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
| 不同时间各物质的物质的量/mol | ||||
| 0min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |
①0min~2min内H2的平均反应速率为0.18mol•L-1•min-1.
②达平衡时,CH4的转化率为20%.在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比变小(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有ad(填字母)
A.CO的含量保持不变 B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变 D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的.工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过).

①a电极的名称为阳极.
②写出除去甲醇的离子方程式6Co3++CH3OH+H2O=6Co2++CO2+6H+.
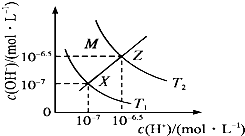
| A. | 由X→Z,c(OH-)增大,所以可以通过加碱来实现 | |
| B. | M区域内任意点均有c(H+)<c(OH-) | |
| C. | T1与T2两条曲线之间的任意点均有c(H+)×c(OH-)=10-14 | |
| D. | XZ线表示c(H+)=c(OH-),溶液显中性,所以XZ线上任意点均有pH=7 |