题目内容
5.下列反应的离子方程式表达正确的是( )| A. | FeC13溶液中滴加HI解液:2Fe3++2HI═2Fe2++2H++I2 | |
| B. | 1mol•L-1NaA1O2溶液和4 mol•L-1HCl溶液等体积混合:AlO2++4H+═Al3++2H2O | |
| C. | NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O | |
| D. | Na2S2O3溶液中滴加过量稀H2SO4:3S2O32-+2H+═4S↓+2SO42-+H2O |
分析 A.HI是可溶性强电解质,应该写离子;
B.二者的物质的量之比为1:4,二者反应生成可溶性的氯化铝、氯化钠和水;
C.NH4HSO4溶液中滴加少量Ba(OH)2溶液,氢氧根离子只和氢离子反应,不和铵根离子反应;
D.二者反应生成硫离子、二氧化硫、硫酸钠和水.
解答 解:A.HI是可溶性强电解质,应该写离子,离子方程式为2Fe3++2I-═2Fe2++I2,故A错误;
B.二者的物质的量之比为1:4,二者反应生成可溶性的氯化铝、氯化钠和水,离子方程式为:AlO2++4H+═Al3++2H2O,故B正确;
C.NH4HSO4溶液中滴加少量Ba(OH)2溶液,氢氧根离子只和氢离子反应,不和铵根离子反,离子方程式为H++SO42-+Ba2++OH-═BaSO4↓+H2O,故C错误;
D.二者反应生成硫离子、二氧化硫、硫酸钠和水,离子方程式为S2O32-+2H+═S↓+SO2↑+H2O,故D错误;
故选B.
点评 本题考查离子方程式正误判断,为高频考点,明确离子方程式书写规则、物质性质、离子反应先后顺序是解本题关键,注意C中离子反应先后顺序、产物与反应物的量有关,注意HI为强电解质、HF为弱电解质,题目难度不大.

练习册系列答案
相关题目
14.在含有大量H+、Ca2+、Cl-溶液中,还可以大量共存的离子是( )
| A. | OH- | B. | CO32- | C. | Ag+ | D. | Mg2+ |
16.下列有关仪器的名称、图形、操作的叙述均正确的是( )
| 选项 | A | B | C | D |
| 名称 | 250mL容量瓶 | 分液漏斗 | 酸式滴定管 | 冷凝管 |
| 图形 |  |  |  | 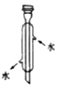 |
| 操作 | 定容时仰视刻度, 则配得的溶液浓 度偏小 | 用酒精萃取水中 碘从上倒出 | 可用于量取 Na2CO3溶液 | 蒸馏实验中将 蒸气冷凝为液体 |
| A. | A | B. | B | C. | C | D. | D |
13.25℃时,下列关系式正确的是( )
| A. | pH=2的CH3COOH 溶液与pH=12的Na0H溶液等体积混合:c(Na+)=c(CH3COO-)>c(CH3COOH) | |
| B. | 盐酸与FeCl3的混合溶液pH=2,稀释10倍后:pH<3 | |
| C. | pH相同的①NH4HSO4、②NH4Cl、③(NH4)2SO4三种溶液的c(NH4+):③>①>② | |
| D. | pH=3的H2C2O4溶液:c(H+)=c(HC2O4-)+c(OH-)=1×10-3mol/L |
20.胡炳成教授团队经过多年的刻苦钻研,通过氧化断裂的方式选择性地切断芳基五唑分子中 的C-N键(如图)首次制得室温下稳定的含能材料(N5)6(H3O)3(NH4)4Cl(PHAC),热分析结果显示PHAC分解温度高达116.8℃,具有非常好的热稳定性.下列说法错误的是( )


| A. | 反应表明拆开N-C键比N-N键容易 | B. | 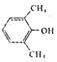 属于芳香醇的异构体有5种 属于芳香醇的异构体有5种 | ||
| C. | PHAC是一种酸式盐 | D. | PHAC能用于制造高能炸药 |
10.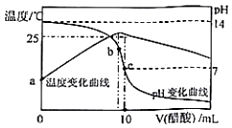 在某温度时,将nmol/L醋酸溶液滴入10mL1.0mol/LNaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol/L醋酸溶液滴入10mL1.0mol/LNaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
 在某温度时,将nmol/L醋酸溶液滴入10mL1.0mol/LNaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )
在某温度时,将nmol/L醋酸溶液滴入10mL1.0mol/LNaOH溶液中,溶液pH和温度随加入醋酸溶液体积变化曲线如图所示,下列有关说法正确的是( )| A. | n>1.0 | B. | a点Kw=1.0×10-14 | ||
| C. | 水的电离程度:c>b | D. | b点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
14.下列有关性质的比较,错误的是( )
| A. | 酸性:H2SO4>H2CO3 | B. | 沸点:CBr4>CCl4 | ||
| C. | 碱性:Al(OH)3>NaOH | D. | 热稳定性:HF>HCl |