题目内容
3.如图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )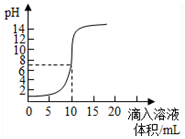
| A. | 原来盐酸的物质的量浓度为0.1mol•L-1 | |
| B. | 可以选择红色石蕊作为指示剂 | |
| C. | 氢氧化钠的物质的量浓度为0.1mol•L-1 | |
| D. | pH为7时加入的氢氧化钠的物质的量为0.1mol |
分析 A.未加NaOH溶液时盐酸pH=1,HCl是强电解质,则c(HCl)=c(H+)=10-pH;
B.石蕊试液的变色范围是5-8;
C.HCl、NaOH都是强电解质,二者完全反应时物质的量之比为1:1,所以溶液pH=7时二者恰好完全反应,则c(HCl).V(HCl)=c(NaOH).V(NaOH);
D.pH=7时n(NaOH)=n(HCl).
解答 解:A.未加NaOH溶液时盐酸pH=1,HCl是强电解质,则c(HCl)=c(H+)=10-pH=10-1 mol/L=0.1mol/L,故A正确;
B.石蕊试液的变色范围是5-8,滴定终点时颜色变化不明显,应该用酚酞作指示剂,故B错误;
C.HCl、NaOH都是强电解质,二者完全反应时物质的量之比为1:1,所以溶液pH=7时二者恰好完全反应,则c(HCl).V(HCl)=c(NaOH).V(NaOH),所以c(NaOH)=$\frac{0.1mol/L×0.1L}{0.01L}$=1mol/L,故C错误;
D.pH=7时n(NaOH)=n(HCl)=0.1mol/L×0.1L=0.01mol,故D错误;
故选A.
点评 本题考查酸碱混合溶液定性判断,侧重考查学生图象分析及计算能力,明确图象中拐点、曲线变化含义是解本题关键,易错点是指示剂的选取,题目难度不大.

练习册系列答案
相关题目
13.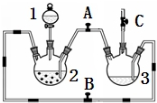 某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
(1)稀硫酸应放在分液漏斗中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B、打开开关AC就可观察到氢氧化亚铁的颜色.试分析实验开始时排尽装置中空气的理由防止生成的氢氧化亚铁被氧化
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是将铁粉换成铁块或铁钉.
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体 (相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
①为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
滴定过程中发生反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色
通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表示).上表中第一次实验中记录数据明显大于后两次,其原因可能是BC
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
 某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.(1)稀硫酸应放在分液漏斗中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B、打开开关AC就可观察到氢氧化亚铁的颜色.试分析实验开始时排尽装置中空气的理由防止生成的氢氧化亚铁被氧化
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是将铁粉换成铁块或铁钉.
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体 (相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇.
①为洗涤(NH4)2SO4•FeSO4•6H2O粗产品,下列方法中最合适的是D
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol•L-1的酸性KMnO4溶液滴定.每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次来 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
滴定终点的现象是最后一滴滴入,溶液由无色变为浅紫色,且30s不变色
通过实验数据计算的该产品纯度为$\frac{980c}{a}$×100%(用字母ac表示).上表中第一次实验中记录数据明显大于后两次,其原因可能是BC
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低.
11.下列反应既是吸热反应,又是氧化还原反应的是( )
| A. | 甲烷在O2中燃烧的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的碳与H2O(g)反应 | D. | 铝片与稀H2SO4反应 |
18.下列离子方程式正确的是( )
| A. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 过氧化钠溶于水:2022-+2H2O═4OH-+O2↑ | |
| C. | 将过量二氧化硫气体通入氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| D. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
15.下列相关实验能达到预期目的是( )
| 选项 | 实验操作 | 实验目的 |
| A. | 可逆反应FeCl3(aq)+3KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化. | 验证浓度对化学平衡的影响 |
| B. | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和硫酸中,观察气泡产生的快慢. | 验证固体接触面积对化学反应速率的影响 |
| C. | 相同温度下,两只试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量MnO2固体. | 验证不同催化剂对H2O2分解速率的影响 |
| D. | 将SO2气体通入溴水中,观察溶液颜色的变化 | 证明SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
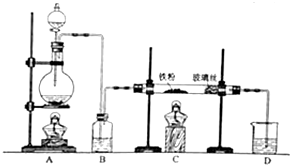 回答下列问题:
回答下列问题: