题目内容
120℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃1L与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,原混合烃中乙炔的体积分数为( )
| A、12.5% | B、25% |
| C、50% | D、75% |
考点:有关混合物反应的计算
专题:计算题
分析:发生反应分别为:C2H6+
O2=2CO2+3H2O,C2H2+
O2=2CO2+H2O,C3H6+
O2=3CO2+3H2O,该条件下水为气态,恢复到原来的温度和压强,根据反应方程式可知,相同体积的C2H6和C3H6反应后体积缩小的量是相同的,故可将两者看成是一种物质,设C2H6和C3H6一共为xmL,C2H2为ymL,利用气体体积不变可知C2H6和C3H6的体积之和与乙炔的体积相等,从而计算乙炔的体积分数.
| 7 |
| 2 |
| 5 |
| 2 |
| 9 |
| 2 |
解答:
解:120℃和101kPa时水的状态为气体,根据燃烧方程式,则:
C2H6+
O2=2CO2+3H2O 增大△V
1 3.5 2 2 0.5
C2H2+
O2=2CO2+H2O 缩小△V
1 2.5 2 1 0.5
C3H6+
O2=3CO2+3H2O 增大△V
1 4.5 3 3 0.5
根据反应方程式可知,相同体积的C2H6和C3H6反应后体积缩小的量是相同的,故可将两者看成是一种物质,设C2H6和C3H6一共为xmL,C2H2为ymL,
则:0.5x=0.5y,
即:原混合烃中乙炔的体积分数为:
×100%=50%,
故选C.
C2H6+
| 7 |
| 2 |
1 3.5 2 2 0.5
C2H2+
| 5 |
| 2 |
1 2.5 2 1 0.5
C3H6+
| 9 |
| 2 |
1 4.5 3 3 0.5
根据反应方程式可知,相同体积的C2H6和C3H6反应后体积缩小的量是相同的,故可将两者看成是一种物质,设C2H6和C3H6一共为xmL,C2H2为ymL,
则:0.5x=0.5y,
即:原混合烃中乙炔的体积分数为:
| 1 |
| 1+1 |
故选C.
点评:本题考查混合物计算,题目难度中等,关键是根据方程式判断体积变化,把C2H6和C3H6看作一个组分,从而转化为两组分混合,注意差量法的应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5mol?L-1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A、1.12g |
| B、6.42g |
| C、2.24g |
| D、3.24g |
分别中和等量的氢氧化钠溶液,需要a mol/L的盐酸、b mol/L的硝酸、c mol/L的硫酸溶液的体积相等,则a、b、c的关系式正确的是( )
| A、a=b=c |
| B、2a=2b=c |
| C、a=b=2c |
| D、都不正确 |
水由于受到有机物污染而造成富营养化,使水中鱼类大批死亡,鱼类死亡是因为( )
| A、藻类大量繁殖,抢走了鱼类的营养 |
| B、水中缺氧,窒息而死 |
| C、水中氧气过多 |
| D、水中含有有毒的金属元素过多 |
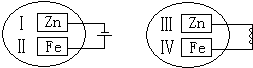 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )| A、Ⅰ附近溶液变红,Zn-2e-=Zn2+ |
| B、Ⅳ附近溶液变红,O2+2H2O+4e-=4OH- |
| C、Ⅱ附近有黄绿色气体生成,2Cl--2e-=Cl2↑ |
| D、Ⅲ附近有无色气体生成,2H++2e-=H2↑ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1 mol?L-1 NaOH溶液:K+、Ba2+、Cl-、HCO3- |
| B、0.1 mol?L-1 Na2CO3溶液:K+、NH4+、NO3-、SO42- |
| C、0.1 mol?L-1 FeCl3溶液:K+、Na+、I-、SCN- |
| D、0.1 mol?L-1 HCl的溶液:Ca2+、Na+、ClO-、NO3- |
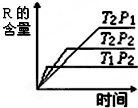 在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )| A、T2>T1,正反应放热,L是液体 |
| B、P2<P1,正反应吸热,L是固体 |
| C、T2<T1,正反应放热,L是气体 |
| D、P2>P1,正反应吸热,L是气体 |
 氟元素半径小,电负性高,可与金属或非金属生成最高价化合物,如MnF2、SF6等.
氟元素半径小,电负性高,可与金属或非金属生成最高价化合物,如MnF2、SF6等. 探究实验发现,硝酸发生氧化还原反应时,浓度越稀,对应还原产物中氮元素的化合价越低.
探究实验发现,硝酸发生氧化还原反应时,浓度越稀,对应还原产物中氮元素的化合价越低.