题目内容
用标准浓度的盐酸滴定未知浓度的氢氧化钠溶液,测定结果,氢氧化钠溶液浓度值偏高,产生误差的原因可能是( )
| A、酸式滴定管用蒸馏水洗涤后,又用标准液润洗 |
| B、滴定过程中锥形瓶中振荡,有液体溅出 |
| C、滴定完毕,滴定管尖端外挂有液滴 |
| D、滴定前仰视读数,滴定终点俯视读数 |
考点:中和滴定
专题:电离平衡与溶液的pH专题
分析:根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差.
| c(标注)×V(标准) |
| V(待测) |
解答:
解:A、酸式滴定管用蒸馏水洗涤后,又用标准液润洗,不影响消耗的标准液的体积,根据c(待测)
分析,可知不影响测定结果,故A错误;
B、滴定过程中锥形瓶中振荡,有液体溅出,导致消耗的标准液体积偏小,根据c(待测)
分析,可知测定结果偏小,故B错误;
C、滴定完毕,滴定管尖端外挂有液滴,导致消耗的标准液体积偏大,根据c(待测)
分析,可知测定结果偏大,故C正确;
D、滴定前仰视读数,滴定终点俯视读数,滴定时消耗的标准液体积偏小,根据c(待测)
分析,可知测定结果偏小,故D错误;
故选C.
| c(标注)×V(标准) |
| V(待测) |
B、滴定过程中锥形瓶中振荡,有液体溅出,导致消耗的标准液体积偏小,根据c(待测)
| c(标注)×V(标准) |
| V(待测) |
C、滴定完毕,滴定管尖端外挂有液滴,导致消耗的标准液体积偏大,根据c(待测)
| c(标注)×V(标准) |
| V(待测) |
D、滴定前仰视读数,滴定终点俯视读数,滴定时消耗的标准液体积偏小,根据c(待测)
| c(标注)×V(标准) |
| V(待测) |
故选C.
点评:本题主要考查了化学实验操作中的误差分析,题目难度中等,掌握实验的原理及正确的误差分析是解题的关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
在下列各溶液中,一定能大量共存的一组离子是( )
| A、含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- |
| B、使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- |
| C、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Na+ |
| D、通有SO2的溶液中:Fe2+、Mg2+、Cl-、SO42- |
Na2CO3、KAlO2、Na2SiO3、Na2SO4溶液,能区分他们的最简单的试剂或方法是( )
| A、焰色反应 | B、盐酸 |
| C、氢氧化钠溶液 | D、水 |
实验测得常温下0.1mol/L某一元酸(HA)溶液的pH值等于1,0.1mol/L某一元碱(BOH)溶液里c(H+)/c(OH-)=10-12.将此两种溶液等体积混合后,所得溶液呈的各离子的浓度由大到小排列的顺序是( )
| A、c(B+)>c(A-)>c(OH-)>c(H+) |
| B、c(A-)>c(B+)>c(H+)>c(OH-) |
| C、c(B+)=c(A-)>c(H+)=c(OH-) |
| D、c(B+)>c(A-)>c(H+)>c(OH-) |
下列说法正确的是( )
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、欲除去Cl2中少量HCl气体,可将此混合气体通过盛饱和食盐水的洗气瓶 |
| C、漂白粉有效成分是CaCl2和Ca(ClO)2,应密闭保存 |
| D、SO2和Cl2都具有漂白作用,所以将两种气体同时作用于潮湿有色物质,可大大增强漂白作用 |

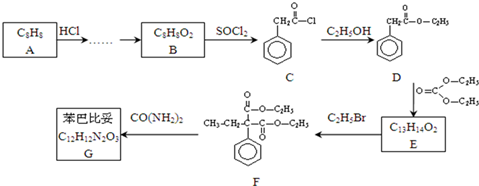



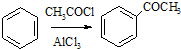 ,请设计合理方案以B的同系物
,请设计合理方案以B的同系物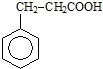 为原料合成
为原料合成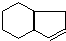 (用合成路线流程图表示为:A
(用合成路线流程图表示为:A