题目内容
4.四种短周期元素在周期表中的相对位置如下所示,其中Z元素最外层电子数是其电子层数的2倍.请回答下列问题:| X | Y | |
| Z | W |
(2)实验室制取X元素的简单氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(3)硒是人体必需的微量元素,与Y同主族,硒原子比Y原子多两个电子层,则硒的原子序数34.
(4)将过量的W的单质通入FeBr2的溶液中,发生反应的离子方程式2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl-.
分析 由短周期元素在周期表中的相对位置,可知X、Y处于第二周期,Z、W处于第三周期,Z元素最外层电子数是其电子层数的2倍,最外层电子数为6,则Z为S元素,可推知W为Cl、Y为O、X为N,据此解答.
解答 解:由短周期元素在周期表中的相对位置,可知X、Y处于第二周期,Z、W处于第三周期,Z元素最外层电子数是其电子层数的2倍,最外层电子数为6,则Z为S元素,可推知W为Cl、Y为O、X为N.
(1)元素Z为S,在周期表中的位置是:第三周期第ⅥA族,
故答案为:第三周期第ⅥA族;
(2)X元素的氢化物为氨气,实验室制取氨气的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(3)硒是人体必需的微量元素,与Y同主族,硒原子比Y原子多两个电子层,则硒的原子序数为8+8+18=34,故答案为:34;
(4)将过量的氯气通入FeBr2的溶液中,发生反应的离子方程式:2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl-,
故答案为:2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl-.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,(4)中注意离子反应的先后顺序与数量关系,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.根据陈述的知识,类推得出的结论正确的是( )
| A. | 钠在空气中燃烧生成的氧化物是Na2O2,则锂在空气中燃烧生成的氧化物是Li2O2 | |
| B. | NH3和PCl3是等电子体,均为三角锥形结构 | |
| C. | CO2和SiO2 化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | 第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 |
13.常温下,0.10mol/L的下列溶液中呈中性的是( )
| A. | 氨水 | B. | NaNO3溶液 | C. | 盐酸 | D. | Na2CO3溶液 |
12.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)根据表中的实验数据,可以得到的结论是其他条件相同时,增大H2C2O4浓度(或反应物浓度),反应速率增大.
(2)表中的V=2.0;利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)=0.01(或1.0×10-2)mol/(L•min).
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
| 1 | 3.0 | V | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
(1)根据表中的实验数据,可以得到的结论是其他条件相同时,增大H2C2O4浓度(或反应物浓度),反应速率增大.
(2)表中的V=2.0;利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)=0.01(或1.0×10-2)mol/(L•min).
19.下列关于碱金属元素的叙述正确的是( )
| A. | 碱金属的密度随着原子序数的递增逐渐减小 | |
| B. | 钾与氧气或水反应比钠与氧气或水反应剧烈,铷、铯的相应反应更剧烈 | |
| C. | 随着原子序数的递增碱金属单质的熔沸点升高 | |
| D. | 碱金属元素阳离子的氧化性随着原子序数的递增依次增强 |
13.以惰性电极电解CuSO4溶液.一段时间后取出电极,加入0.1molCu(OH)2固体后溶液与电解前相同,则电解时电路中流过的电子为( )
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3 | D. | 0.4 mol |
14.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、HCO3- | |
| B. | 酸性溶液中可能大量存在Na+、IO3?、SO42-、I? | |
| C. | 碱性溶液中可能大量存在Na+、K+、SO32-、S2- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、Cl?、SO42? |
 .
.
 .
.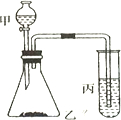 比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实验试剂,利用所给装置验证你的结论(提示:难溶于水).实验试剂:浓盐酸、稀H2SO4、饱和Na2SO3溶液、大理石、Na2CO3粉末、Na2SiO3溶液.实验装置:如图所示
比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实验试剂,利用所给装置验证你的结论(提示:难溶于水).实验试剂:浓盐酸、稀H2SO4、饱和Na2SO3溶液、大理石、Na2CO3粉末、Na2SiO3溶液.实验装置:如图所示