题目内容
10.12.8g铜和浓HNO3反应,随反应进行,产生气体的颜色逐渐变浅,铜完全反应时,收集到标准状况下的气体6.72L,将气体与一定体积的O2同时通入水中可被完全吸收.(1)通过计算确定收集到的气体成分及物质的量.
(2)O2在标准状况下的体积.
分析 (1)铜和浓HNO3反应随反应的进行硝酸浓度变稀,产生气体是一氧化氮和二氧化氮的混合气体,根据得失电子守恒分析解答;
(2)根据电子守恒计算,已知HNO3$\stackrel{Cu}{→}$NO、NO2$\stackrel{氧气}{→}$HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,以此进行计算.
解答 解:(1)设气体中NO2、NO的物质的量分别为x、y.
气体的体积为6.72L,则$x+y=\frac{6.72L}{22.4L/mol}$,有得失电子守恒有:$x+3y=\frac{12.8g}{64g/mol}×2$;
解之得x=0.25 mol; y=0.05 mol;
则:NO20.25 mol,NO 0.05mol,
答:集到的气体中NO20.25 mol,NO 0.05mol;
(2)根据铜失去的电子等于氧气得到的电子,则有:${V_{O_2}}=2×\frac{12.8g}{64g/mol}$÷4×22.4 L/mol=2.24 L,答:O2在标准状况下的体积为2.24 L.
点评 本题考查氧化还原反应电子转移数目的计算,本题难度不大,根据HNO3$\stackrel{Cu}{→}$NO、NO2$\stackrel{氧气}{→}$HNO3,得出Cu失去电子数目等于O2得到电子的数目是解答本题的关键.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
20.下面有关苯酚的叙述,其中正确的组合是( )
①是有机化工原料; ②易溶于水也易溶于乙醇; ③可以使紫色石蕊溶液变红; ④酸性比甲酸、乙酸、碳酸均弱;⑤不能和硝酸发生反应; ⑥常温下易被空气氧化; ⑦既可以和H2发生加成反应,又可以和溴水发生取代反应;⑧纯净的苯酚是粉红色的晶体;⑨苯酚有毒,沾到皮肤上可用浓氢氧化钠溶液洗涤;⑩苯酚能与FeCl3溶液反应生成紫色沉淀.
①是有机化工原料; ②易溶于水也易溶于乙醇; ③可以使紫色石蕊溶液变红; ④酸性比甲酸、乙酸、碳酸均弱;⑤不能和硝酸发生反应; ⑥常温下易被空气氧化; ⑦既可以和H2发生加成反应,又可以和溴水发生取代反应;⑧纯净的苯酚是粉红色的晶体;⑨苯酚有毒,沾到皮肤上可用浓氢氧化钠溶液洗涤;⑩苯酚能与FeCl3溶液反应生成紫色沉淀.
| A. | ①③⑥⑦⑧ | B. | ①②③④⑦ | C. | ①④⑥⑦ | D. | ①④⑥⑦⑩ |
5.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液.下列说法正确的是( )
| A. | 元素Y的最高正化合价为+6 | B. | 离子半径的大小顺序为W>Q>Z>X>Y | ||
| C. | 工业上用电解法冶炼Z单质 | D. | 元素Q的含氧酸的酸性一定比W的强 |
15.在一定条件下,可以用如图(1)所示的硼化钒(VB2)-空气电池(工作时反应为:4VB2+11O2═4B2O3+2V2O5)为电源给图(2)所示装置通电,模拟有机物的电化学储氢.下列说法正确的是( )
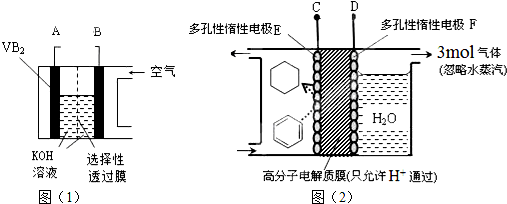

| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
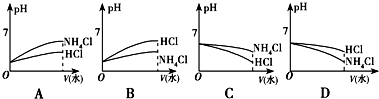
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
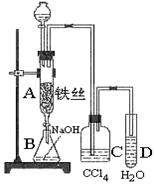 某化学课外小组用图装置使苯与液溴反应.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用图装置使苯与液溴反应.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.