题目内容
A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A的原子结构示意图为: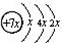 .B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
.B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A B C D
(2)上述五种元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 (填化学式)
(3)D所在周期(除稀有气体元素外)第一电离能最大的元素是 ,电负性最大的元素是
(4)D的氢化物的电子式为
(5)C、D的氢化物,相同条件下在水中的溶解度更大的是 ,原因是
(6)E元素+3价阳离子的核外电子排布式是 .
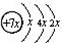 .B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
.B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
(2)上述五种元素的最高价氧化物对应水化物中,酸性最强的是
(3)D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物的电子式为
(5)C、D的氢化物,相同条件下在水中的溶解度更大的是
(6)E元素+3价阳离子的核外电子排布式是
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D是四种短周期元素,由A的原子结构示意图可知,x=2,A的原子序数为14,故A为Si元素;A、B、C同周期,B是同周期第一电离能最小的元素,故B为Na元素,C的最外层有三个成单电子,故C原子的3p能级有3个电子,故C为P元素;C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,E的核外电子排布式为1s22s22p63s23p63d64s2,则E为Fe元素.
解答:
解:A、B、C、D是四种短周期元素,由A的原子结构示意图可知,x=2,A的原子序数为14,故A为Si元素;A、B、C同周期,B是同周期第一电离能最小的元素,故B为Na元素,C的最外层有三个成单电子,故C原子的3p能级有3个电子,故C为P元素;C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,则E为Fe元素.
(1)由上述分析可知,A为Si元素、B为Na元素、C为P元素、D为N元素.故答案为:Si;Na;P;N;
(2)非金属越强最高价氧化物对应水化物酸性越强,非金属性N>P>Si,酸性最强的是HNO3;金属性越强最高价氧化物对应水化物碱性越强,金属性Na最强,碱性最强的是NaOH,故答案为:HNO3;NaOH;
(3)同周期自左而右,第一电离能增大(个别除外),所以第一电离能最大的元素是F,周期自左而右,电负性增大,故电负性最大的元素是F,故答案为:F;F;
(4)D的氢化物为NH3,电子式为 ,故答案为:
,故答案为: ;
;
(5)C、D的氢化物分别为PH3、NH3,NH3与水分子间能形成氢键,增大了溶解度,故答案为:NH3;NH3与水分子间能形成氢键,增大了溶解度;
(6)E元素+3价阳离子为Fe3+,Fe为26号元素,Fe3+核外电子排布式是1s22s22p63s23p63d5,故答案为:1s22s22p63s23p63d5.
(1)由上述分析可知,A为Si元素、B为Na元素、C为P元素、D为N元素.故答案为:Si;Na;P;N;
(2)非金属越强最高价氧化物对应水化物酸性越强,非金属性N>P>Si,酸性最强的是HNO3;金属性越强最高价氧化物对应水化物碱性越强,金属性Na最强,碱性最强的是NaOH,故答案为:HNO3;NaOH;
(3)同周期自左而右,第一电离能增大(个别除外),所以第一电离能最大的元素是F,周期自左而右,电负性增大,故电负性最大的元素是F,故答案为:F;F;
(4)D的氢化物为NH3,电子式为
 ,故答案为:
,故答案为: ;
;(5)C、D的氢化物分别为PH3、NH3,NH3与水分子间能形成氢键,增大了溶解度,故答案为:NH3;NH3与水分子间能形成氢键,增大了溶解度;
(6)E元素+3价阳离子为Fe3+,Fe为26号元素,Fe3+核外电子排布式是1s22s22p63s23p63d5,故答案为:1s22s22p63s23p63d5.
点评:本题考查元素推断、元素周期律、常用化学用语等,难度不大,推断元素是解题的关键,注意熟练掌握元素周期律与物质性质的递变规律.

练习册系列答案
相关题目
能证明淀粉已经完全水解的试剂是( )
| A、新制的氢氧化铜悬浊液 | B、银氨溶液 |
| C、碘水 | D、碘化钾 |
把0.05molNaOH晶体分别加入到下列100mL液体中,溶液导电性变化最大的是( )
| A、0.5mol?L-1NH4Cl |
| B、0.5mol?L-1醋酸 |
| C、0.5mol?L-1H2SO4 |
| D、0.5mol?L-1Cu(NO3)2 |
某条件下,锌与稀硝酸反应,其物质的量之比为5:12,则此时硝酸的还原产物是( )
| A、NO2 |
| B、N2O |
| C、N2 |
| D、NH4NO3 |
下列说法正确的是( )
| A、P的非金属性比N强,对应的单质白磷比氮气活泼 |
| B、工业上通常用电解Na、Fe、Cu对应的氯化物制得该三种金属单质 |
| C、氨易液化、硫化氢在同族元素的氢化物中熔沸点最低可用同一原理解释 |
| D、Cl、Br、I的非金属性逐渐减弱,HCl、HBr、HI水溶液的酸性逐渐减弱 |
下列物质的分类合理的是( )
| A、碱性氧化物:Na2O、CaO、MgO、Na2O2 |
| B、碱:NaOH、KOH、Ba(OH)2、Na2CO3 |
| C、铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3?H2O |
| D、非金属氧化物:CO2、NO、SO2、H2O |