题目内容
17.(1)等质量的O2和O3,它们的物质的量之比为3:2,所含分子数之比为3:2,所含原子数之比为1:1,相同状况下的体积之比和密度之比分别为3:2、2:3.(2)在标准状况下,空气中N2和O2的体积比约为4:1,则N2和O2的物质的量之比为4:1,空气的密度约为1.29g•L-1,空气的平均相对分子质量为29.
分析 (1)根据n=$\frac{m}{M}$可知,等质量的O2和O3,它们的物质的量之比与摩尔质量成反比;根据N=nNA可知,分子数目之比等于物质的量之比;O2和O3均由O原子构成,二质量相等,含有氧原子数目相等;相同条件下,体积之比等于物质的量之比,根据$ρ=\frac{m}{V}$,质量相同,密度之比与体积成反应比;
(2)在标准状况下,N2和O2的物质的量之比为体积之比,空气的平均相对分子质量等于质量比总物质的量,根据$ρ=\frac{M}{V}$计算.
解答 解:(1)根据n=$\frac{m}{M}$可知,等质量的O2和O3,它们的物质的量之比=48g/mol:32g/mol=3:2;
根据N=nNA可知,O2和O3所含分子数目之比=O2和O3物质的量之比=3:2;
O2和O3均由O原子构成,二质量相等,含有氧原子数目相等,即含有氧原子数目之比为1:1;
相同条件下,O2和O3体积之比=O2和O3的物质的量之比=3:2,根据$ρ=\frac{m}{V}$,质量相同,密度之比与体积成反应比,所以密度之为
2:3,故答案为:3:2;3:2;1:1;3:2;2:3;
(2)在标准状况下,N2和O2的物质的量之比为体积之比,则N2和O2的物质的量之比为4:1,M=$\frac{4×28+1×32}{5}$=29,所以空气的密度约为$\frac{29}{22.4}$=1.29g•L-1,故答案为:4:1;1.29g•L-1;29.
点评 本题考查物质的量有关计算,注意对公式的理解与灵活应用,侧重对基础知识的巩固,题目难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
7.分别依据下列实验事实,得出的结论正确的是( )
| 实验事实 | 结论 | |
| A | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 | 随溶液pH减小,“84”消毒液的氧化能力增强 |
| B | 苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 | 苯酚的酸性比碳酸强 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向1 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1 mol/LNaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L NaBr溶液,有淡黄色沉淀生成 | 氯化银的溶解度小于溴化银 |
| A. | A | B. | B | C. | C | D. | D |
5.下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:则下列说法正确的是( )
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g)△H1 | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g)△H2 | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O (g)?CO2(g)+H2(g)△H3 | K3 | ? | ? |
| A. | △H1<0,△H2>0 | |
| B. | 反应①②③的反应热满足关系:△H2-△H1=△H3 | |
| C. | 反应①②③的平衡常数满足关系:K1•K2=K3 | |
| D. | 要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施 |
12.下列实验对应的现象及结论均正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将过量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 浓硫酸滴入蔗糖中,并搅拌 | 得黑色蓬松的固体并有刺激性气味气体 | 该过程中浓硫酸仅体现吸水性和脱水性 |
| C | 向FeCl2溶液中加入足量Na2O2粉末 | 出现红褐色沉淀和无色气体 | FeCl2溶液部分变质 |
| D | 向过量FeI2溶液中先滴加几滴淀粉溶液,再滴加几滴新制氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
2.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A. | 2H2(g)+O2(g)═2H2O(l);△H1 2H2(g)+O2(g)═2H2O(g);△H2 | |
| B. | S(g)+O2(g)═2SO2(g);△H1 S(s)+O2(g)═2SO2(g);△H2 | |
| C. | C(s)+$\frac{1}{2}$ O2(g)═CO(g);△H1 C(s)+O2(g)═CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$ Cl2(g)═HCl(g);△H2 |
9.等物质的量的氢气和氦气在同温同压下具有相等的( )
| A. | 原子数 | B. | 体积 | C. | 中子数 | D. | 质量 |
6.下表为各物质中所含有的少量杂质以及除去这些杂质所选用的试剂或操作方法.下列表述正确的是( )
| 序号 | A | B | C | D |
| 物质 | KNO3溶液 | CO2 | 水 | 乙醇 |
| 杂质 | KOH | H2O(g) | 溴 | 水 |
| 除杂试剂 | FeCl3溶液 | - | 乙醇 | 生石灰 |
| 除杂 装置 | 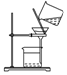 | 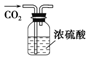 | 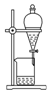 | 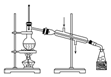 |
| A. | A | B. | B | C. | C | D. | D |
7.下列有关气体摩尔体积的描述中正确的是( )
| A. | 相同物质的量的气体摩尔体积一定相同 | |
| B. | 通常状况下的气体摩尔体积约为22.4L | |
| C. | 标准状况下的气体摩尔体积约为22.4L | |
| D. | 单位物质的量的气体所占的体积就是气体摩尔体积 |