题目内容
9.下列实验操作能达到目的是( )| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| B. | 制取二氧化氮时,用水或NaOH溶液吸收尾气 | |
| C. | 为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg,该方案可行 | |
| D. | 为测定镀锌铁皮的锌层厚度,将镀锌铁皮与足量盐酸反应待气泡明显减少时取出,洗涤,烘干,称重.若烘干时间过长,会导致测定结果偏小 |
分析 A.钠元素焰色反应呈黄色,但溶液中的溶质不一定是钠盐;
B.二氧化氮和水反应生成硝酸和NO;
C.应先把水蒸气排除才合理;
D.烘干时间过长,使剩余物的质量偏大,锌的质量偏小.
解答 解:A.钠元素焰色反应呈黄色,但溶液中的溶质不一定是钠盐,可能是NaOH,故A错误;
B.二氧化氮和水反应生成硝酸和NO,NO不能被水吸收,故B错误;
C.混合物与足量稀硫酸充分反应,也会生成水和二氧化,所以逸出的气体是二氧化碳,但会混有水蒸气,即碱石灰增加的质量不是二氧化碳的质量,不能测定含量,故C错误;
D.烘干时间过长,使剩余物的质量偏大,锌的质量偏小,则测定结果偏小,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及焰色反应、尾气处理、物质含量测定等知识点,明确实验原理及物质性质是解本题关键,注意C中排除其它因素干扰,为易错点.

练习册系列答案
相关题目
19.关于NO的下列叙述不正确的是( )
| A. | NO不溶于水,是一种大气污染物 | |
| B. | NO是一种红棕色的有毒气体 | |
| C. | NO结合血红蛋白的能力比CO还强 | |
| D. | NO与氧气反应生成NO2,体现其还原性 |
20.下列实验目的可以实现或操作正确的是( )
| A. | 用托盘天平称取3.23 g NaCl固体 | |
| B. | 用10 mL 量筒量取 7.50 mL 稀盐酸 | |
| C. | 分液以后 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 | |
| D. | 粗盐提纯中除泥沙的操作顺序是:溶解、过滤、蒸发 |
17. 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
(1)一定温度下,在2L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应.10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为20%.
(2)如图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,写出该反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234KJ/mol
(3)在容积恒定的密闭容器中,进行如下反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
①写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$;
②试判断K1>K2(填写“>”“=”或“<”);
③NH3(g)燃烧的方程式为4NH3(g)+7O2(g)═4NO2(g)+6H2O(l),已知:
2H2(g)+O2(g)═2H2O(l)△H=-483.6kJ/mol N2(g)+2O2(g)═2NO2 (g)△H=+67.8kJ/mol
N2(g)+3H2(g)═2NH3 (g)△H=-92.0kJ/mol 则NH3 (g)的燃烧热282.8kJ/mol.
(4)常温1L0.1mol•L-1醋酸与1L0.1mol•L-1氨水反应,放出的热量为a kJ,写出此离子反应的热化学方程式CH3COOH(aq)+NH3•H2O(aq)=CH3COO-(aq )+NH4+ (aq )+H2O(l)△H=-10akJ/mol.
 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.(1)一定温度下,在2L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应.10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为20%.
(2)如图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,写出该反应的热化学方程式:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234KJ/mol
(3)在容积恒定的密闭容器中,进行如下反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
| T/K | 398 | 498 |
| 平衡常数K | K1 | K2 |
②试判断K1>K2(填写“>”“=”或“<”);
③NH3(g)燃烧的方程式为4NH3(g)+7O2(g)═4NO2(g)+6H2O(l),已知:
2H2(g)+O2(g)═2H2O(l)△H=-483.6kJ/mol N2(g)+2O2(g)═2NO2 (g)△H=+67.8kJ/mol
N2(g)+3H2(g)═2NH3 (g)△H=-92.0kJ/mol 则NH3 (g)的燃烧热282.8kJ/mol.
(4)常温1L0.1mol•L-1醋酸与1L0.1mol•L-1氨水反应,放出的热量为a kJ,写出此离子反应的热化学方程式CH3COOH(aq)+NH3•H2O(aq)=CH3COO-(aq )+NH4+ (aq )+H2O(l)△H=-10akJ/mol.
14.将磷肥生产中形成的副产物石膏(CaSO4•2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图.
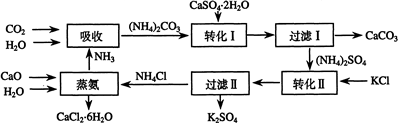
(1)本工艺中所用的原料除CaSO4•2H2O、KCl外,还需要CaCO3、(或CaO)、NH3、H2O等原料
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:
CaSO4+CO32-=CaCO3+SO42-
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有CaSO4(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32-的方法是:取少量溶液,滴加稀盐酸,若有气泡产生则还含有CO32-,
反之则不含有CO32-.
(5)已知不同温度下K2SO4在100g水中达到饱和时溶解的量如表:
60℃时K2SO4的饱和溶液591g冷却到0℃,可析出K2SO4晶体54g
(6)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是Ad
A、熔点较低(29℃熔化) b、能导电 c、能制冷 d、无毒
(7)上述工艺流程中体现绿色化学理念的是:碳酸钙用于制水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用等
原子利用率高,没有有害物质排放到环境中.

(1)本工艺中所用的原料除CaSO4•2H2O、KCl外,还需要CaCO3、(或CaO)、NH3、H2O等原料
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:
CaSO4+CO32-=CaCO3+SO42-
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有CaSO4(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32-的方法是:取少量溶液,滴加稀盐酸,若有气泡产生则还含有CO32-,
反之则不含有CO32-.
(5)已知不同温度下K2SO4在100g水中达到饱和时溶解的量如表:
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
(6)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是Ad
A、熔点较低(29℃熔化) b、能导电 c、能制冷 d、无毒
(7)上述工艺流程中体现绿色化学理念的是:碳酸钙用于制水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用等
原子利用率高,没有有害物质排放到环境中.
18.下列说法或表示方法正确的是( )
| A. | 由C(石墨)=C(金刚石)△H=+11.9 kJ/mol,可知金刚石比石墨稳定 | |
| B. | 等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量多 | |
| C. | 水力(水能)按不同的分类可看成可再生能源和一级能源 | |
| D. | 可表示氢气燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol |
19.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-=Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-=H2O 2KOH+H2SO4═K2SO4+2H2O |
